



新冠的爆发让mRNA技术从各种疫苗技术中脱颖而出,也推动了mRNA疫苗的商业化,辉瑞/BioNTech以及Moderna的两款mRNA疫苗的相继获批上市,mRNA疫苗未来将会有更广阔的发展空间。随着越来越多的mRNA疫苗应用于临床,疫苗的有效性和安全性评价也更加需要重视。
01
mRNA疫苗作用机制

mRNA疫苗将特异性抗原的部分mRNA引入人体细胞内,利用宿主细胞的蛋白质合成机制产生抗原,从而激发特异性免疫反应,并达到形成免疫记忆的效果。mRNA疫苗可分为预防性传染病mRNA疫苗和治疗性肿瘤mRNA疫苗。预防性传染病mRNA疫苗在细胞中表达传染病特异抗原,激活机体的免疫应答反应产生抗体,从而达到预防传染性疾病的目的。治疗性肿瘤mRNA疫苗是在机体细胞内合成肿瘤特异性抗原蛋白,诱导机体产生免疫应答反应,从而有针对性地攻击肿瘤细胞,达到肿瘤预防或治疗的作用。
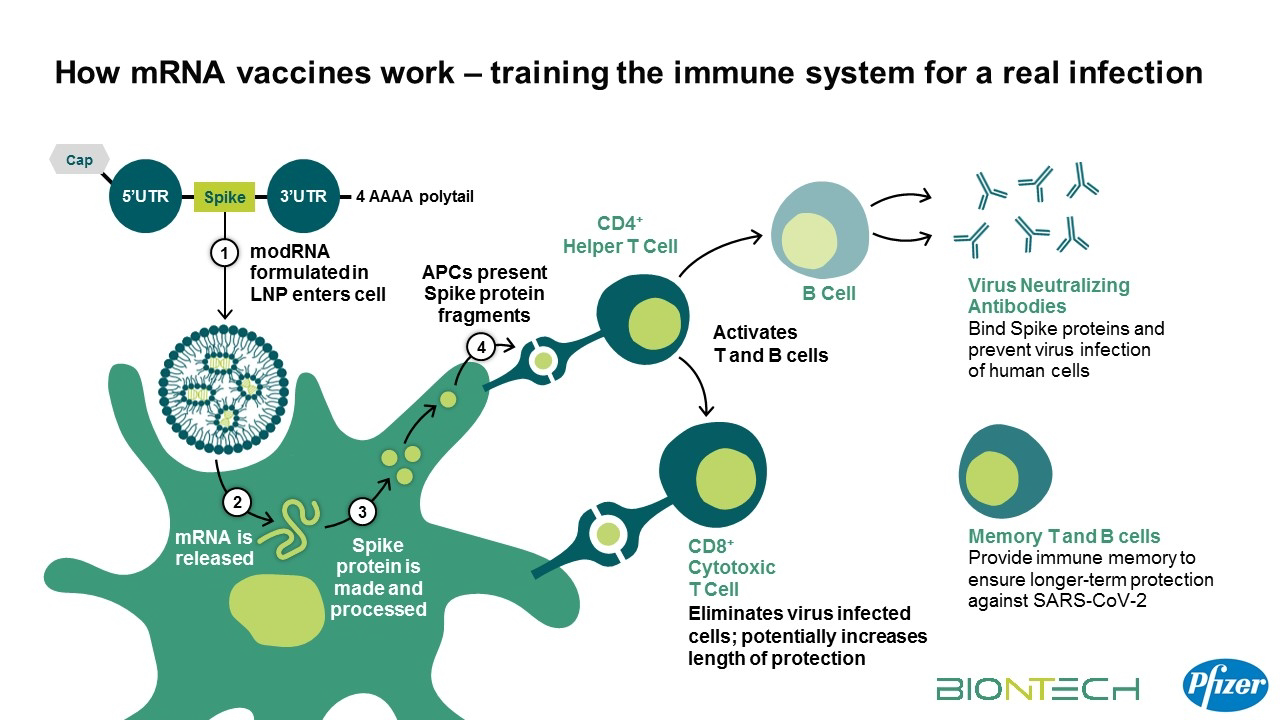
图1 mRNA疫苗作用机制
如图所示,mRNA疫苗从合成到启动免疫反应主要经历以下三个阶段,包括体外mRNA合成、细胞内加工和启动免疫反应。mRNA疫苗被封装在脂质体(LNP)载体纳米颗粒中,并被抗原呈递细胞内吞,mRNA从载体逃逸后释放到细胞质中,然后由核糖体翻译成抗原蛋白。随后,内源性抗原被蛋白酶体降解为多肽,由MHC I呈递并激活细胞毒性T细胞(CD8+T细胞)。此外,分泌的抗原可被细胞吸收,在内切体内降解,并通过MHC II类蛋白在细胞表面呈现给辅助性T细胞。最后,辅助性T细胞(CD4+T细胞)刺激B细胞产生抗病原体的中和抗体。
02
mRNA疫苗优势

· 有效性高:一次给药,可表达多种抗原,免疫原性强,可激活细胞免疫和体液免疫;
· 安全性高:不存在潜在宿主感染风险或整合到宿主细胞基因组中的诱变风险,自我降解可通过正常生理过程代谢;
· 研发周期短:平台技术复用性强,能更有效应对突发疫情或病毒变异;
· 低生产成本+快生产速度:体外转录合成制备,无需细胞培养和动物源基质,生产线可复用可快速制备。通常传统疫苗的生产至少需要6个月时间,而mRNA疫苗由于高产量的体外转录反应和快速制剂的特点,在实现标准化生产的情况下30天内就可产成,疫苗的时效性在应对突发疫情尤其是病毒变异时分外重要。
03
mRNA疫苗应用

mRNA技术在理论上可以生产出任何一种人类所需的蛋白质。除新冠疫苗外,mRNA疫苗广泛应用于传染病预防研究,如预防呼吸道合胞病毒(RSV)、巨细胞病毒(CMV)、寨卡病毒、流感病毒、狂犬病毒等传染性疾病领域。Moderna宣布RSV mRNA疫苗mRNA-1345的三期临床达到主要终点,对于2种或2种以上症状的保护率为83.7%,mRNA-1345为表达pre-F蛋白的单价mRNA疫苗,进行单次免疫,根据该数据,Moderna将于2023年递交上市申请。
mRNA疫苗能够更精准地靶向特异免疫目标。筛选出肿瘤相关抗原进行测序、分析,将对应的mRNA序列合成疫苗,使自身细胞生产出抗原标识物,并以此激发对应的特异性免疫。由于mRNA疫苗中的编码可以进行编辑,可以准确地控制产生的抗原蛋白种类和序列,选择仅仅在肿瘤细胞中才会分泌的抗原蛋白标志物作为靶点,避免误伤其他正常细胞,使特异免疫精准地靶向肿瘤。此外,mRNA 疫苗能够激发针对细胞的T细胞免疫,在杀伤肿瘤细胞方面拥有更高的效率。
mRNA-4157(个体化肿瘤疫苗)是针对每位肿瘤患者量身定制的个体化肿瘤疫苗,能够容纳高达34个编码新抗原的mRNA序列,注射到患者体内后,mRNA上携带的指令就会告诉患者的癌细胞表达所选的新表位,进而患者自身的免疫系统能够识别出癌细胞并精准的杀伤肿瘤细胞。Merck与Moderna联合开发的个体化癌症疫苗mRNA-4157正与Merck的PD-1抗体(Keytruda)联用,应用于完全切除的黑色素瘤患者的辅助治疗。临床试验结果显示,与单独使用Keytruda相比,联合治疗将复发或死亡的风险降低了44%, FDA 已授予“突破性治疗”认定,用于高危黑色素瘤患者接受完全切除术后的辅助治疗,此次认定意味着mRNA疗法可能成为治疗黑色素瘤和其他癌症的新兴前沿疗法。
04
mRNA疫苗的免疫原性评估

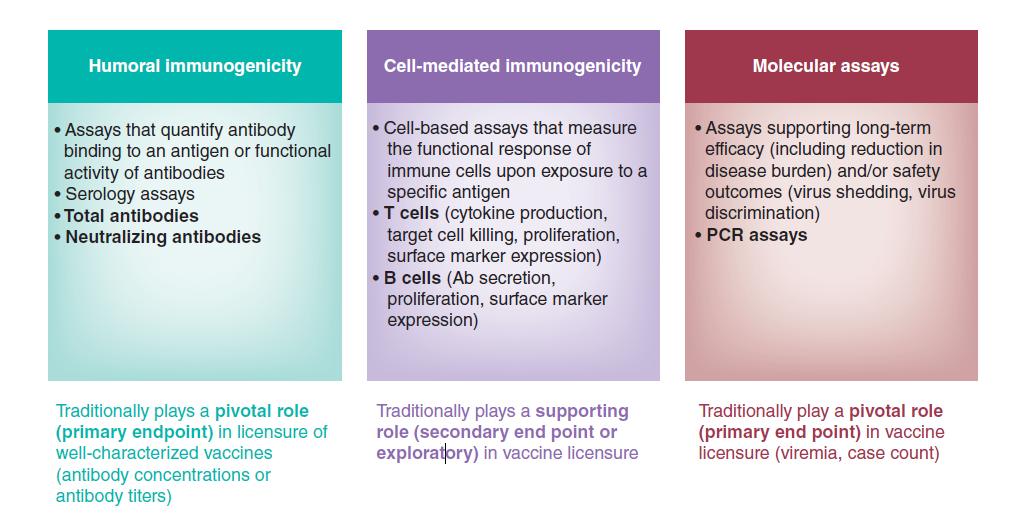
图2 疫苗研发中涉及的不同类型的生物分析方法
免疫原性是疫苗研发各个阶段需要关注的重要指标,包括疫苗的免疫原性评价以及有效性评价。以辉瑞/BioNTech新冠mRNA疫苗为例,COVID-19 mRNA疫苗的有效性和安全性分析如下:
· ELISA/Luminex检测血清中抗体针对COVID-19病毒Spike蛋白及RBD区域的结合作用;
· 疫苗诱导的中和抗体应答通过COVID-19病毒中和试验和假病毒中和试验检测;
· IFN-γ ELISPOT检测PBMC的免疫响应(使用Spike重组糖蛋白分别刺激疫苗接种前后同一志愿者体内PBMC,对比接种后和接种前细胞分泌IFN-γ程度);
· 流式细胞术检测CD4+ T cell及CD8+ T cell经Spike重组糖蛋白刺激后产生的IL-2、IFN-γ及TNFα;
· MSD/Luminex验证细胞因子检测;

图3 mRNA疫苗临床生物分析内容
(以辉瑞/BioNTech新冠mRNA疫苗为例)
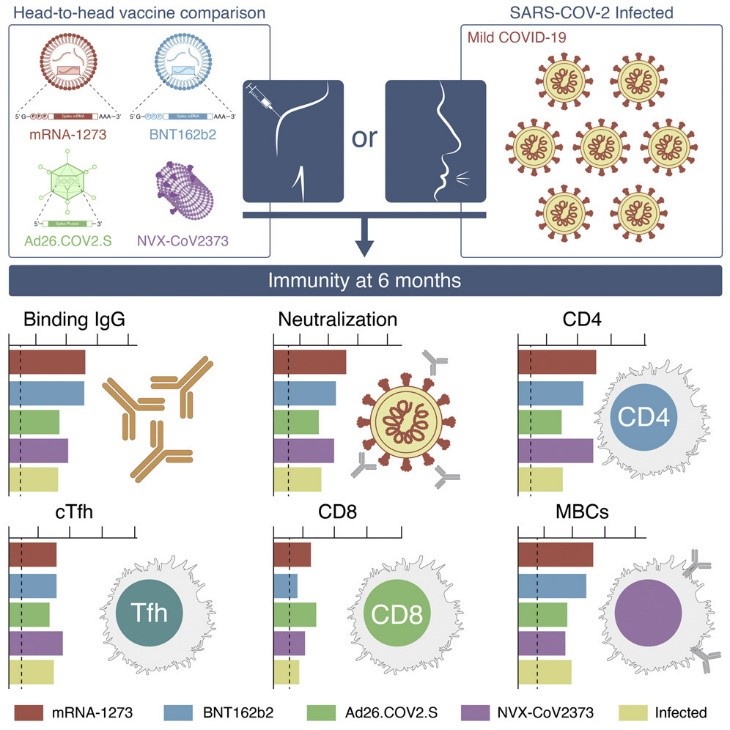
图4 四种新冠疫苗诱导的体液和细胞免疫
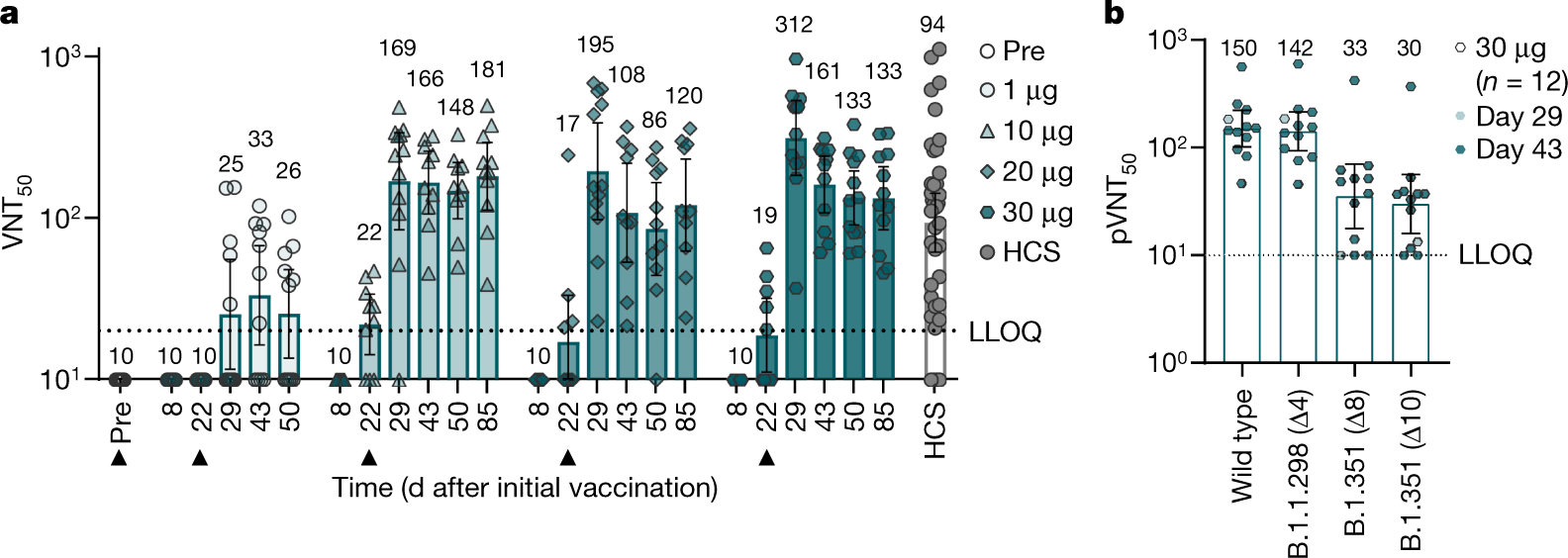
图5 BNT162b2诱导IgG抗体和病毒中和抗体
结合抗体和中和抗体常用于mRNA疫苗的免疫原性和保护效力分析,BNT162b2疫苗1/2期临床试验结果发现BNT162b2产生了强烈新冠抗体反应,SARS-CoV-2人体血清中有50%的中和几何平均滴度(GMT)是COVID-19人群恢复期样本(HCS)中观察到的3.3倍。BNT162b2诱导血清中和了22种含有SARS-CoV-2S变体的假病毒。
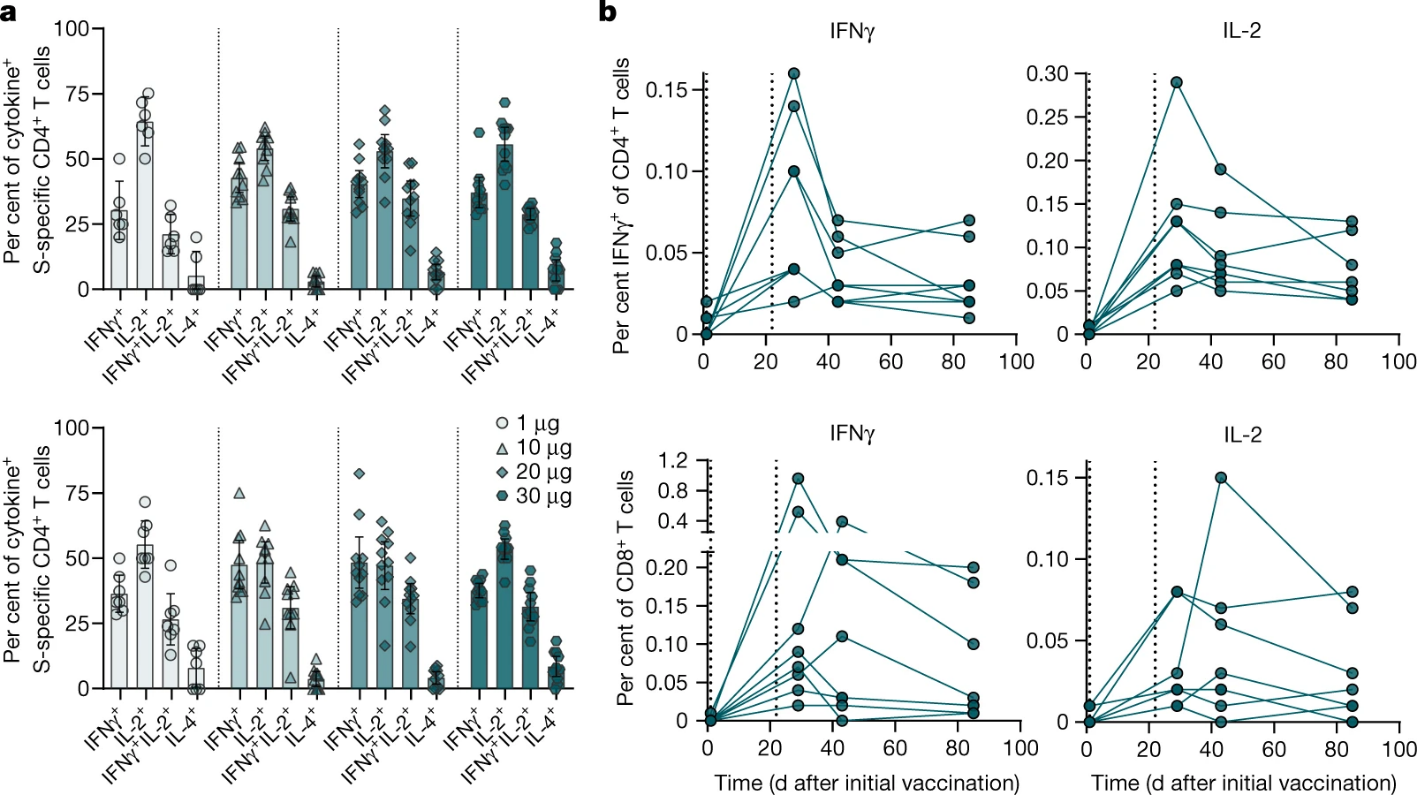
图6 BNT162b2诱导T细胞分泌细胞因子
细胞免疫的作用机制主要是包括两个方面,致敏T细胞的直接杀伤作用,以及其通过释放细胞因子的协同作用,因此mRNA疫苗细胞免疫分析为细胞免疫表型及胞内细胞因子检测、监测疫苗接种后的安全性,通常采用流式细胞术(FACS)或酶联免疫斑点技术(ELISPOT)来进行检测。
BNT162b2临床试验中,大多数参与者具有强烈的IFNγ或IL-2阳性CD8+和CD4+T细胞反应,并在9周后的整个观察期内仍能检测到。一周后,表位特异性CD8+早期分化的效应器记忆表型T细胞占总循环CD8+的0.02-2.92%,8周后检测到0.01-0.28%。总之,BNT162b2在人体内可诱导产生中和抗体以及多特异性细胞免疫反应。
05
总结与经验

熙宁生物|精翰生物拥有完善的技术平台和丰富的经验,可为mRNA疫苗临床前以及临床阶段提供一站式的生物分析服务。包括mRNA基因水平检测(qPCR),表达产物水平和功能活性检测(Bioassay/ELISA/MSD),抗病毒结合抗体和抗病毒中和抗体检测(Cell Based Assay/LBA),细胞免疫反应(ELISPOT/FACS)以及细胞因子(ELISA/MSD/Luminex)等,高效助力mRNA药物研发。
熙宁生物 免疫分析平台介绍
支持产品类型:
蛋白药(单抗,双抗,融合蛋白,ADC,融合蛋白等),细胞和基因治疗药物
可检测项目:
药代动力学(PK),药效学(PD)
抗药抗体(ADA),中和抗体(NAb)
生物标志物(Biomarker),细胞因子

熙宁生物 流式细胞术检测细胞亚群经验
• 检测CD45、CD3、CD4、CD8、CD19,CD56等指标 (TBMNK)
• 检测CD3、CD4、CD8、CD19、CD56、CD25、CD127等指标 (TBNK, Treg)
• 检测CD3、CD4、CD8、CD16、CD56,Ki67等指标 (Ki67)
• 检测CD3、CD4、CD8、中心记忆细胞、效应记忆细胞( CD45RA, CCR7)
• 检测CD3、CD4、CD8、PD-1、LAG3、TIM3、 中心记忆细胞、效应记忆细胞
• 检测CD3、CD4、CD8、Treg、NK、 Ki67等指标 (细胞增殖)
• 检测CD3、CD4、CD8、CD25、CD69、HLA-DR (T细胞激活)
• 检测CD3、CD4、CD8、4-1BB、ICOS (T细胞激活)
• 检测BCMA、CD19 、CD38、CD138、CD56、CD117
• 检测骨髓克隆性浆细胞含量(CD45、CD19、D38、CD56、CD138)
• 检测淋巴细胞亚群分型(CD19 、CD22 、CD38、CD138、CD56、CD117)
• 检测淋巴细胞亚群分型(BCMA、CD19 、CD38、CD138、CD56、CD117)
• 检测CD45、CD38、CD138、CD19、CD117、CD81、BCMA、Kappa、Lambda、CD56、CD27
• 检测CD19、CD45、CD38、CD56、CD20、CD138、CD269、k轻链、λ轻链
• 检测 CD45、CD3、CD4、CD8、CD19、CD56、CD25、CD127、CD45RA、CCR7、PD-1、TIGIT、TIM3、LAG3、CD27、CD69、CD38、HLR-DR、4-1BB
06
参考文献

1. mRNA-based modalities for infectious disease management
2. 2020 White Paper on Recent Issues in Bioanalysis: Vaccine Assay Validation, qPCR Assay Validation, QC for CAR-T Flow Cytometry, NAb Assay Harmonization and ELISpot.
3. mRNA-based therapeutics: powerful and versatile tools to combat diseases
4. Development of functionally relevant potency assays for monovalent and multivalent vaccines delivered by evolving technologies
5. BNT162b2 vaccine induces neutralizing antibodies and poly-specific T cells in humans