



前言
补体系统是天然免疫的重要部分,在病原体免疫监测和维持组织稳态中起着重要作用。补体系统识别免疫复合物、受损细胞或病原微生物的分子信号,继而触发蛋白水解级联反应。该级联反应由三条途径组成,分别称为经典途径、凝集素途径和替代途径(CP、LP和AP)。补体系统的过量激活或者失调可能导致一系列的疾病发生。 随着Alexion研发的首款C5补体抑制剂Sorilis以及后续长效的C5补体抑制剂Ultomiris的成功,Apellis研发的首款C3补体抑制剂Empavel成功上市,补体系统的药物研发成为越来越热的赛道。本文简单盘点下目前补体系统药物研发的热门靶点,从临床前和临床阶段药效学分析方法的角度介绍下基于人血清/红细胞裂解的补体功能药效学测定旁路途径检测分析。
补体抑制剂药物研发进展
针对补体系统的过量激活开发了大量的补体信号通路关键分子的抑制剂,目前走在前列的是靶向C5,C3,C1S等抑制剂已成功上市,适应症主要集中在PNH, aHUS, myasthenia gravis等领域,同时随着新药研发的进程,在一期二期临床阶段,靶向FactorB,FactorD, MASP2补体系统新型抑制剂也在快速推进,部分补体系统的药物研发见图1,补体药物正当时。
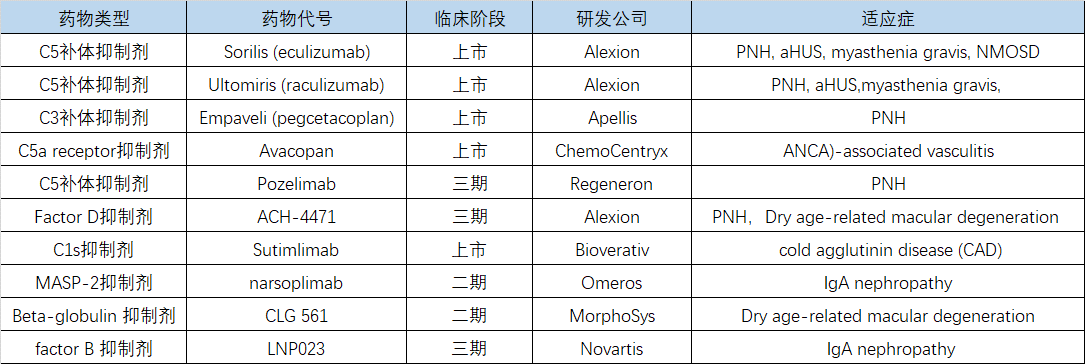
图1:补体抑制剂的研发进展
补体抑制剂作用机理和药效学分析方法
如图2所示,补体系统的激活主要由三条路径组成:
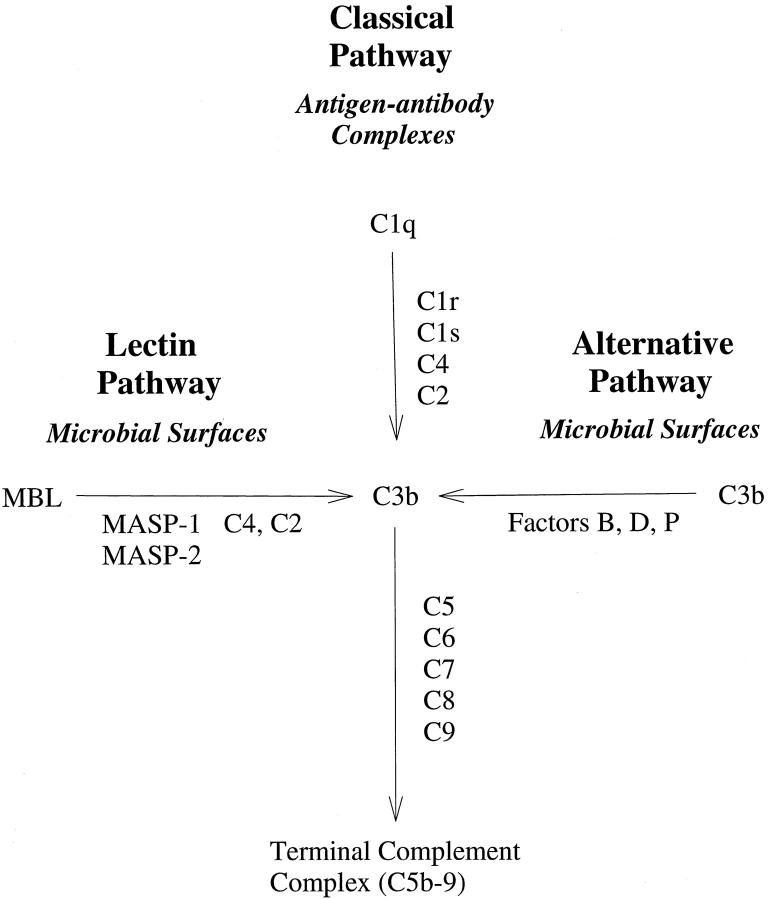
图2:补体系统的三条激活路径
1. 经典途径(CP):
经典途径需要机体的抗体(通常为IgM,或者多聚化的IgG)和特定的抗原形成复合物后启动,首先被补体系统中的识别单位:包括C1q、C1r、C1s识别;然后通过活化单位:包括C2、C3、C4形成级联反应,最后由膜攻击单位:包括C5、C6、C7、C8和C9,通过蛋白水解酶的作用形成复核物结合到细胞膜,使细胞膜损伤破碎。
2. 凝集素途径 (LP):
凝集素途径由机体的甘露聚糖结合凝集素(mannan-binding lectin,MBL)或纤维胶凝蛋白(ficolin,FCN)直接识别多种病原微生物表面的甘露糖、N-乙酰甘露糖、N-乙酰葡萄糖氨、岩藻糖等为末端糖基的糖结构。MBL-MASP复合物与病原体表面糖结构结合,使MASP-1、MASP-2被独立地激活。活化的MASP2发挥其活性,裂解C4,所产生的C4b片段共价结合于病原体表面,通过与C2相互作用,使后者也被MASP2裂解,形成C3转化酶C4b2a,继之活化补体CP;活化的MASP1能直接裂解C3产生C3b,在fD和fP的作用下,形成C3转化酶C3bBb或C3bBbP,并产生C5转化酶C3bBb3b,激活补体AP。
3. 旁路途径 (AP):
旁路途径在正常生理情况下,机体的C3与B因子、D因子等相互作用,可缓慢的产生极少量的C3B和C3bBb(旁路途径的C3转化酶),但迅速受H因子和I因子的作用,不再能激活C3和后续的补体成分。
旁路途径的激活在于激活物质(例如细菌脂多糖、肽聚糖;病素感染细胞、肿瘤细胞,痢疾阿米巴原虫等)的出现。激活物质的存在为C3b或C3bBb提供不易受H因子置换Bb,不受Ⅰ因子灭活C3b的一种保护性微环境,使旁路激活途径从和缓进行的准备阶段过渡到正式激活的阶段。
当C3被激活物质激活时,其裂解产物C3b又可在B因子和D因子的参与作用下合成新的C3bBb。后者又进一步使C3裂解。由于血浆中有丰富的C3,又有足够的B因子和Mg2 ,因此这一过程一旦被触发。就可能激活的产生显著的扩大效应。有人称此为依赖C3Bb的正反馈途径,或称C3b的正反馈途径,激活效应将持续扩大。
在进行补体系统的新药研发过程中,针对不同的药物靶点,因处于补体激活信号通路的不同位置,甚至其靶向的补体路径不一样,需要采用不同的补体激活药效血评估方法进行评估,这需要基于药物的作用机理和补体激活路径的充分了解下进行选择;同时由于补体激活的三条激活路径在活化和膜攻击进程中会共用部分信号分子,检测方法的特异性需要进行充分的评估。
C3抑制剂Empaveli的临床药效学分析方法解析
上市药物Empaveli的药物作用机理如图3靶向补体蛋白C3,阻断C3进一步活化,从而抑制补体信号通路的激活。由于C3蛋白的活化是经典路径,凝集素路径和旁路途径共有,Empaveli可以同时抑制三条补体激活信号通路,跟三条信号通路相关的活性分析方法均能够表征其药效。
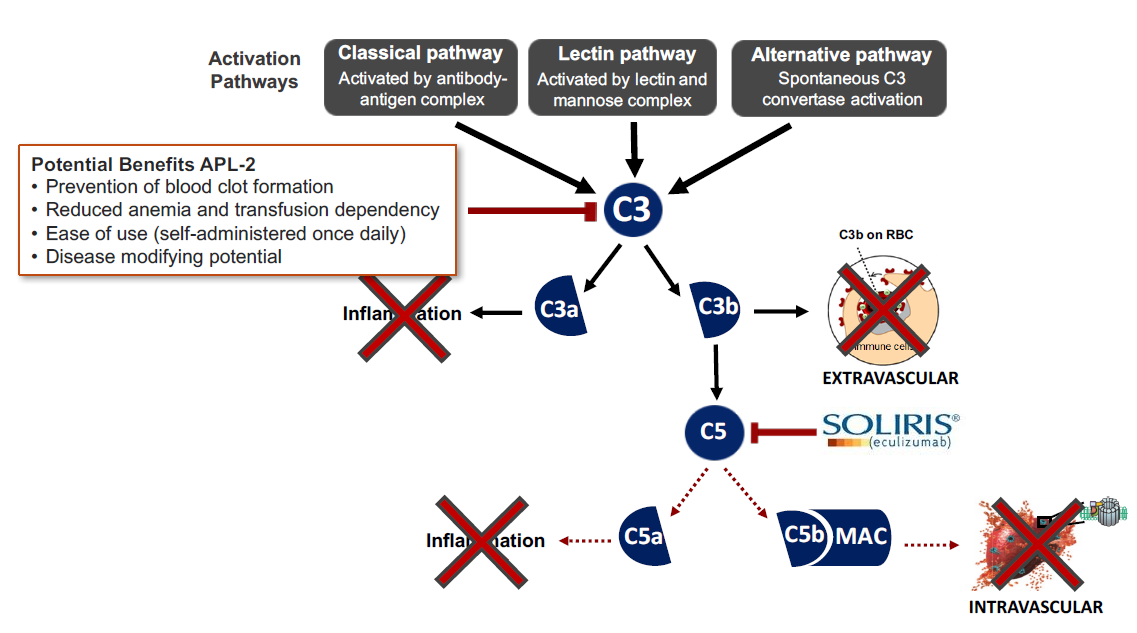
图3:Empaveli的药物作用机理
从Empaveli披露的文献信息,其药效学检测分析方法只要进行了C3活性,CH50和AP50的检测。

从Empaveli公布临床前前的药效学数据来看主要的依据是旁路途径的溶血试验抑制效果。
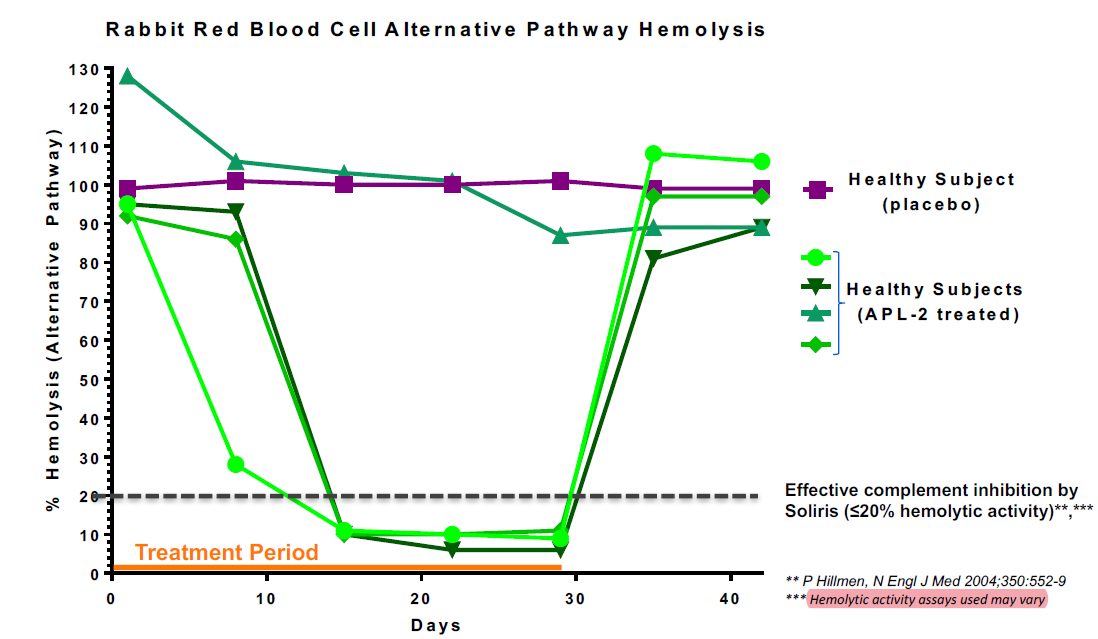
图4:Empaveli临床药效学数据
临床阶段的旁路途径的溶血试验的难点分析:
1. 旁路途径溶血试验相对于经典途径溶血试验,没有加特异性的抗体形成复核物激活C1q,溶血的效果相对较差,方法的区分度会较差。
2. 旁路途径溶血试验没有标准品进行检测体系变化的校准,采用不同来源,不同批次的sheep红细胞,样品血清的检测溶血结果可能会有差异。
3. 不同个体旁路途径的活性不一样,药物引起的效果将不太一样,个体差异较大。可能会出现低活性个体没有药效的情况。(如图4,个别健康个体用药后,药物对个体的旁路补体活性无显著性影响)
4. 旁路途径为无标准品的非定量实验,不同分析批的结果可能会有比较大的差异,在进行临床用药前和用药后的样品进行旁路活性比较时,分析批间的差异将会较大的影响的结果。
5. 旁路途径溶血试验的特异性需要得到证明,以避免经典途径和凝集素途径的干扰
熙宁生物的补体系统临床前和临床药效学分析服务
熙宁生物有丰富的临床阶段基于人血清样品进行补体信号通路药效学评估的方法开发,验证和样品分析的经验。可提供补体激活信号通路中经典途径,凝集素途径和旁路途径的药效学分析服务,部分药效学分析结果如下:
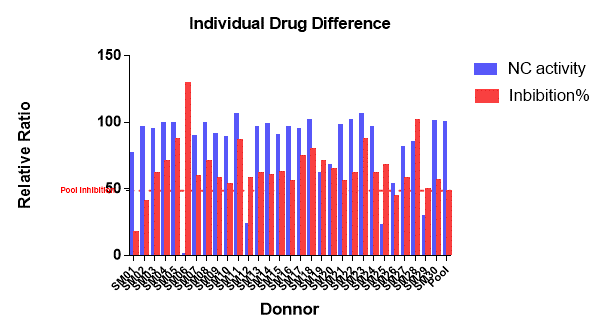
如上图人血清中的补体功能有显著性的个体差异,在进行药效学检测数据分析时需基于个体的补体功能,对药物的效果和离群值进行有效的区分。
基于人血清的补体信号通路药效学评估模型可对药物首次人体用药的剂量进行外推和预测,是临床前转化医学研究到临床阶段早期药效评估的重要桥梁。