



近年来,随着生物技术的发展,体外嵌合抗原受体T细胞(ex vivo CAR-T)在改善血液系统恶性肿瘤,特别是B细胞恶性肿瘤中显示出卓越的疗效。但是其广泛应用面临巨大挑战,原因在于其制备流程复杂且耗时、生产成本高昂、需要高度专业化的设施等因素。此外,患者在接受治疗前还需要进行淋巴清除化疗,增加了治疗的复杂性并带来了潜在的副作用。相比之下,in vivo CAR-T通过定向递送编码CAR的核酸,直接对机体免疫细胞进行工程化改造,简化了复杂的体外CAR-T细胞制造过程,省去了限制可及性的物流环节,而且不需要清淋预处理,充分释放了CAR-T疗法的治疗的潜力。从2024年开始,各大MNC合作或收购了多家专注于体内CAR-T的Biotech,纷纷看好in vivo CAR-T赛道。
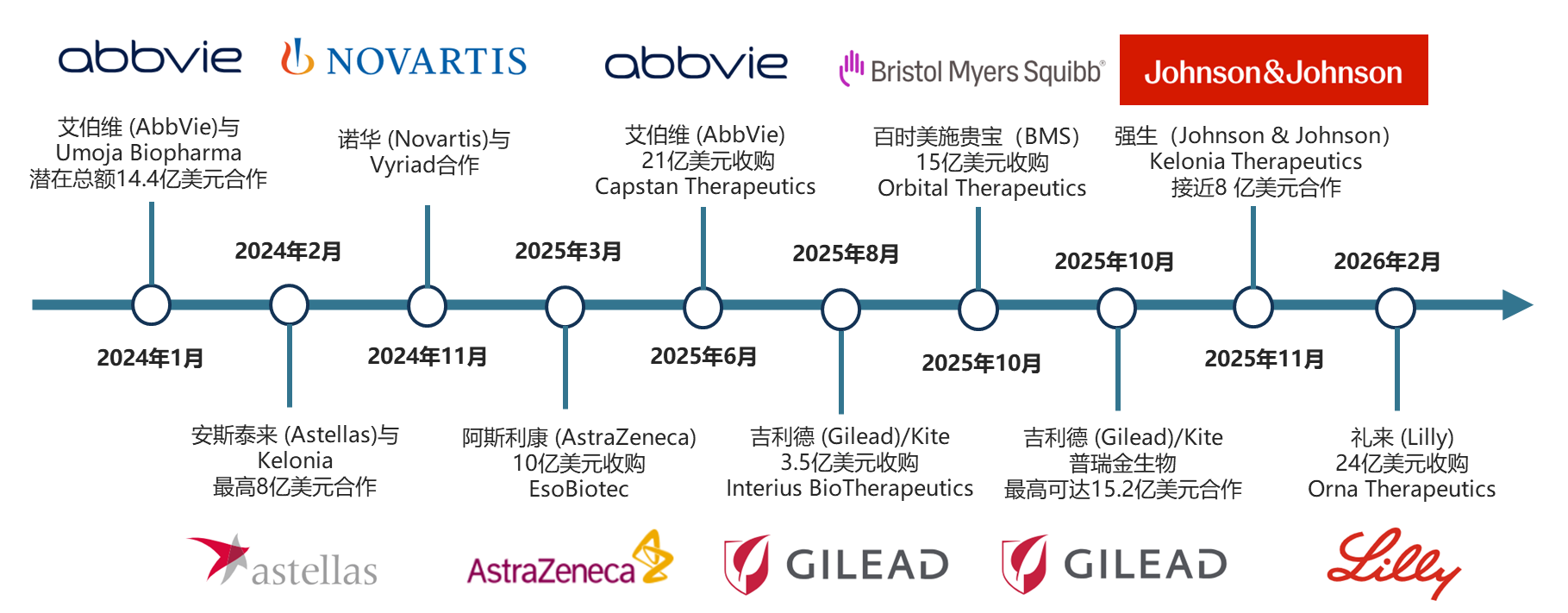
In vivo CAR-T MNC合作与收购概览
2025年年底开始,EsoBiotec(ESO-T01)、Kelonia(KLN-1010)和虹信生物(HN2301)等公司纷纷公布了早期临床的结果,标志着in vivo CAR-T进入快速发展的阶段。此类药物通过递送遗传物质至体内细胞,在体内生成CAR-T,类似基因治疗药物。从药效作用物质和作用机制来看,其通过体内生成的基因修饰细胞发挥治疗作用,类似细胞治疗药物。而且涉及病毒、纳米脂质体等多种类型载体,因此in vivo CAR-T 兼具基因治疗药物和细胞治疗药物双重属性,涉及一系列复杂且动态的生物学过程,这为临床生物分析带来了挑战。
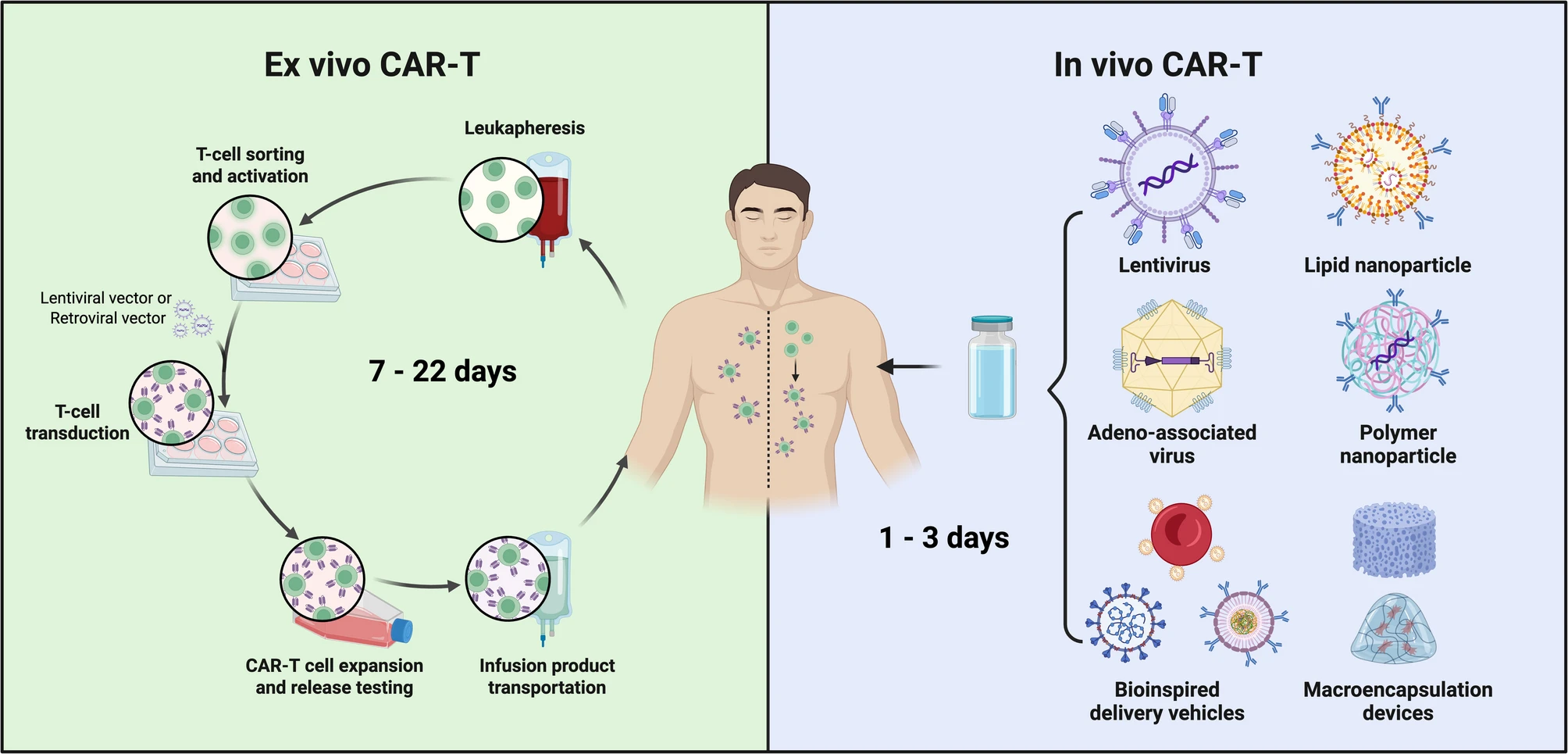
In vivo CAR-T vs Ex vivo CAR-T
本文系统阐述in vivo CAR-T的临床生物分析策略,并以慢病毒载体和mRNA-LNP(脂质纳米颗粒)技术路线为例展开具体分析,为此类产品的临床评价提供参考。
细胞治疗产品的体内过程是影响有效性和安全性的重要因素,应根据具体产品采用适宜的分析方法考察药代动力学特征。In vivo CAR-T进入人体后,病毒载体或者LNP会靶向T细胞,在体内完成T细胞的改造,改造后的CAR-T细胞再对目标细胞进行攻击,因此药代动力学需要从载体层面和细胞层面进行评估。
载体层面,如果使用慢病毒载体,药代动力学可以使用qPCR或dPCR平台,检测血浆中病毒RNA的拷贝数,评估含基因组的慢病毒颗粒。PCR法通常以慢病毒载体基因组中的保守区为靶标,能够快速高灵敏的定量检测血浆中的病毒总颗粒数,是目前常用的检测方法。此外,也可以使用ELISA的方法,针对慢病毒颗粒的P24蛋白进行物理滴度的检测。如果使用LNP递送载体,除了可以使用与慢病毒类似的PCR方法检测递送的mRNA或环状RNA,也可以通过LC-MS/MS针对LNP进行检测,关注LNP在人体内的浓度变化、分布和清除过程。或通过ELISA检测LNP靶向T细胞的抗体片段。
细胞层面,与ex vivo CAR-T类似,免疫细胞在体内一般经历分布、增殖、耗竭等过程,通常采用基于表型检测的流式细胞术和基于分子检测的PCR方法评估细胞动力学。流式分析的过程中,在样品中加入计数磁珠的方式,从而实现对于CAR-T细胞的定量分析。qPCR或dPCR方法通过检测整合至基因组中的病毒拷贝数从而实现定量分析。mRNA-LNP并不发生整合,所以仅能通过流式细胞术评估CAR+细胞动力学。虽然in vivo CAR-T疗法直接注射工程化慢病毒或者LNP,不需要体外对免疫细胞进行工程化改造,但仍需要制备CAR+细胞作为流式和PCR方法学开发的质控品。

熙宁|精翰生物qPCR和dPCR平台
药效学主要研究细胞治疗产品对机体的作用、潜在机制及其定量规律。通常可根据细胞治疗产品的靶点、作用机制及适应症的疾病特点等选择药效学指标。In vivo CAR-T药效学的检测指标,基本上和ex vivo CAR-T一致。细胞治疗产品通常依赖细胞因子实现其效应功能,可以通过MDS平台检测IL-6、IFNs、TNFs和IL-2等细胞因子来评价T细胞的活化特性。通过流式细胞术可以对T淋巴细胞亚群分析,如记忆表型分析以评估长期治疗效果。B细胞恶性肿瘤或自身免疫性疾病可以针对B淋巴细胞亚群分析以评估药物的治疗效果。B/T细胞恶性肿瘤还可以通过NGS或流式细胞术的方法检测微小残留病灶,从而评估患者疾病情况和治疗响应。这些数据均可以对细胞治疗产品的有效性提供有意义的数据支持。


熙宁|精翰生物流式平台
免疫细胞治疗产品可能引起患者的体液和/或细胞免疫反应,并可能因此改变暴露水平,体液免疫产生的抗药抗体可能通过降低细胞治疗产品相应结构域与配体(或靶)结合的能力,进而影响有效性和安全性。In vivo CAR-T外源组分和表达产物均可能引起免疫反应,例如慢病毒、LNP、CAR结构和翻译后修饰、共表达产物等。因此,建议对外源组分和表达产物均进行免疫原性检测方法的开发。
通常采用配体结合分析法,如ELISA、电化学发光法等评估体液免疫风险,常见的开发模式是采用桥连法,能够特异性的检测相关的ADA。针对病毒和LNP本身,通常评估慢病毒包膜糖蛋白(如VSV-G)、衣壳蛋白(P24)、慢病毒/LNP偶联的靶向T细胞结构(如CD3、CD4、CD5、CD7、CD8和TCR等抗体结构域),以及LNP-PEG(特别是PEG的修饰成分)。针对CAR结构,需了解包含与抗原靶点结合区域的生物学功能,如评估与CAR中单链可变区片段(single chain fragment variable,scFv)区域组成的胞外结构域(extracellular domain,ECD)的结合抗体,由于ECD结构域包含与肿瘤抗原靶点结合的区域,因此评估针对该结构域的免疫反应可以了解体液免疫原性对产品疗效的潜在影响。
当存在细胞免疫原性风险时,需进行抗CAR的细胞免疫检测。抗CAR的细胞免疫常通过细胞功能性实验监测。可采用酶联免疫斑点法、流式细胞术检测胞内细胞因子或胞外活化标志物、或其他合适的细胞功能实验分析抗CAR的细胞免疫。



熙宁|精翰生物免疫平台
无论是体内还是体外细胞治疗产品,慢病毒载体会随机整合在T细胞基因组。特别是在癌相关基因的功能区发生的整合,需要特别关注。通常使用NGS的方法对整合位点的多样性和偏好性进行统计学评估以表征安全性风险。在CAR-T细胞治疗产品的制备过程中,具有污染复制型慢病毒(Replication Competent Lentivirus,RCL)的潜在风险。RCL通过病毒载体回复突变产生,是具有复制能力的病毒,所以需要使用qPCR平台检测RCL。此外,还需要使用qPCR/dPCR平台对唾液、尿液和粪便等样本进行病毒脱落的检测,检测方法类似药代动力学血浆病毒拷贝数检测。目前普遍认为脂质纳米颗粒(LNP)的安全性是优于慢病毒载体的,mRNA等转染细胞后是瞬时表达,无插入突变风险。无论是慢病毒还是LNP递送载体,细胞因子的检测不仅是药效学指标,也是安全性指标。



熙宁|精翰生物NGS平台
除了前文已介绍的药效学标志物外,生物标志物的检测通常针对适应症有不同的检测策略。例如针对自身免疫性疾病系统性红斑狼疮,可以检测患者自身抗体和疫苗保护性抗体,以及B细胞受体多样性评估和亚型转换等。检测需要根据疾病相关的生物标志物进行设计和探索,此处不再赘述。生物标志物的方法学验证需要按照fit-for-purpose原则进行。
In vivo CAR-T 作为新兴技术,兼具基因治疗和细胞治疗产品双重属性,同时涉及到不同类型的递送载体,其“体内生成”的特性带来比传统体外细胞治疗产品更加复杂的研究与评价的挑战,因此,开展系统且严谨的生物分析和生物标志物研究将有助于药物安全性和有效性评估。熙宁|精翰生物依托PCR、FACS、LC-MS/MS、ELISA、MSD、NGS及IHC/mIHC等多元化技术平台,可全面支持in vivo CAR-T项目的PK、PD及相关生物标志物全流程检测分析。
目前,公司已累计支持超110个CGT研发管线,凭借深厚的项目经验、完善的技术体系与专业化运营能力,可高效助力申办方加速in vivo CAR-T项目的研发与临床转化进程。
欢迎后台咨询。
参考文献:
[1] Xu J, Chen Z, Su L, Ren A, Mei H. In vivo CAR cell therapy: from bench to bedside. J Hematol Oncol. 2025;18(1):105. Published 2025 Nov 20.
[2] Xu J, Liu L, Parone P, et al. In-vivo B-cell maturation antigen CAR T-cell therapy for relapsed or refractory multiple myeloma. Lancet. 2025;406(10500):228-231.
[3] https://keloniatx.com/kelonia-therapeutics-announces-late-breaking-oral-presentation-of-first-in-human-data-from-in-vivo-bcma-car-t-therapy-at-the-american-society-of-hematology-ash-2025-annual-meeting/
[4] Wang Q, Xiao ZX, Zheng X, et al. In Vivo CD19 CAR T-Cell Therapy for Refractory Systemic Lupus Erythematosus. N Engl J Med. 2025;393(15):1542-1544.
[5] 国家药品监督管理局药品审评中心. 国家药监局药审中心关于发布《细胞治疗产品临床药理学研究技术指导原则(试行)》的通告(2024年第49号)[EB/OL]. 北京:国家药品监督管理局药品审评中心,2024-11-15.