



细胞疗法正在经历第二次革命——从复杂的体外制造转向直接的体内重编程。 随着体内嵌合抗原受体(Chimeric Antigen Receptor,CAR)T细胞治疗技术的发展,该疗法已开始进入临床阶段。首先在恶性肿瘤和自身免疫病中探索工程化慢病毒载体和脂质纳米颗粒(Lipid Nanoparticle,LNP)-mRNA制剂,临床病例研究显示出良好的安全性、耐受性以及生物学应答或临床疗效。
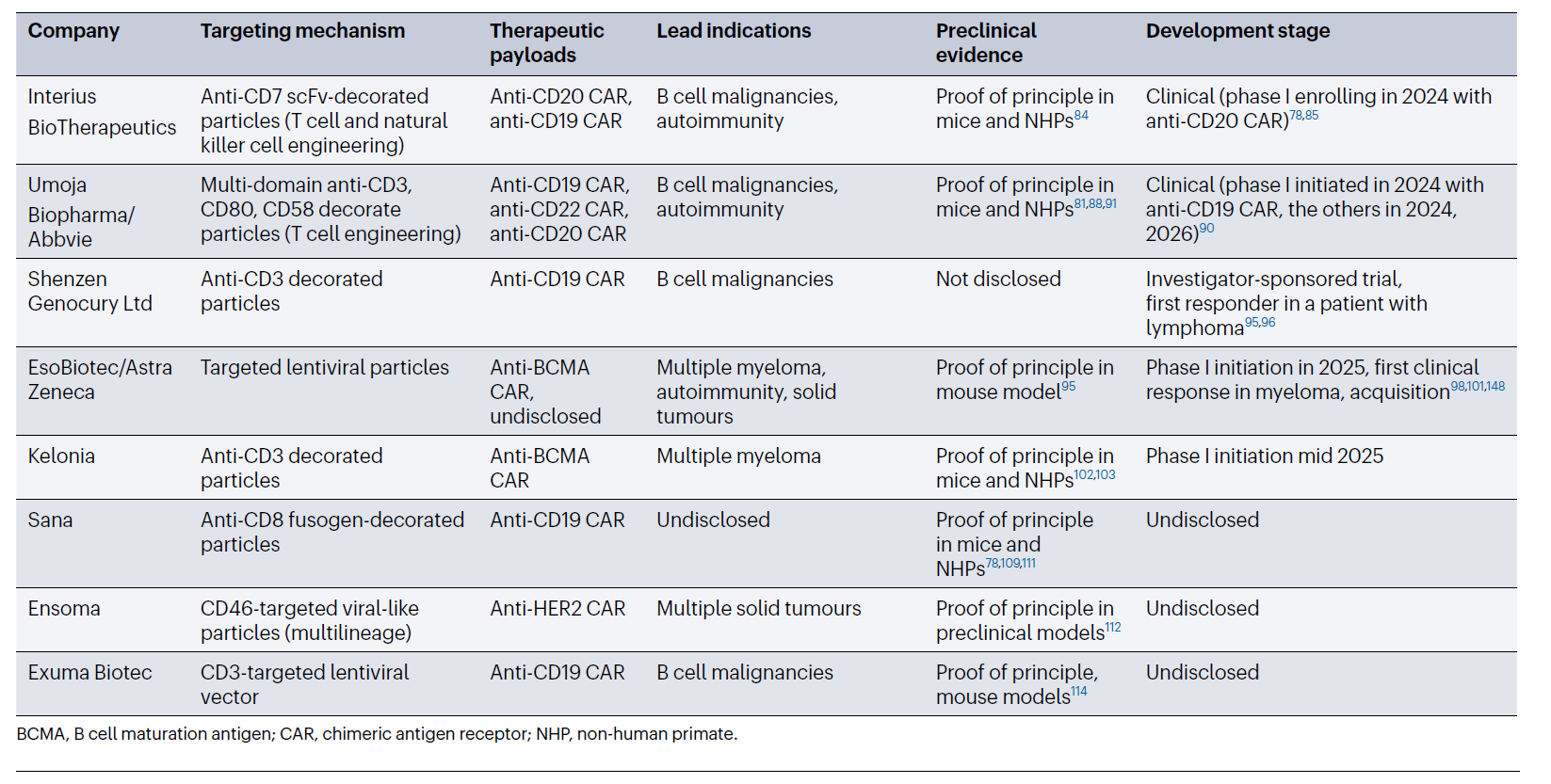
表1 慢病毒体内CAR-T细胞平台汇总
Interius BioTherapeutics的首个临床候选产品INT2104是一种靶向CD7的慢病毒载体,旨在递送抗CD20 CAR,用于治疗B细胞恶性肿瘤。INT2104的精准体内靶向包括CD4+和CD8+T细胞亚群和自然杀伤细胞,单次静脉给药后即可生成多样化的效应性抗CD20 CAR细胞群体。研究人员在非人灵长类动物和人源化小鼠模型中开展了INT2104的体内研究,结果证实INT2104静脉给药后可实现对T细胞和自然杀伤细胞的特异性转导,生成具有功能的抗CD20 CAR细胞并持续存在,且能特异性清除CD20+ B细胞。在食蟹猴中开展的毒理学研究表明,INT2104耐受性良好,静脉给药后未观察到毒性、CRS或神经毒性,2024年10月,INVISE试验的首例受试者完成给药,这是首次人体I期临床试验,评估INT2104静脉输注治疗复发/难治性B细胞恶性肿瘤成人患者的安全性。
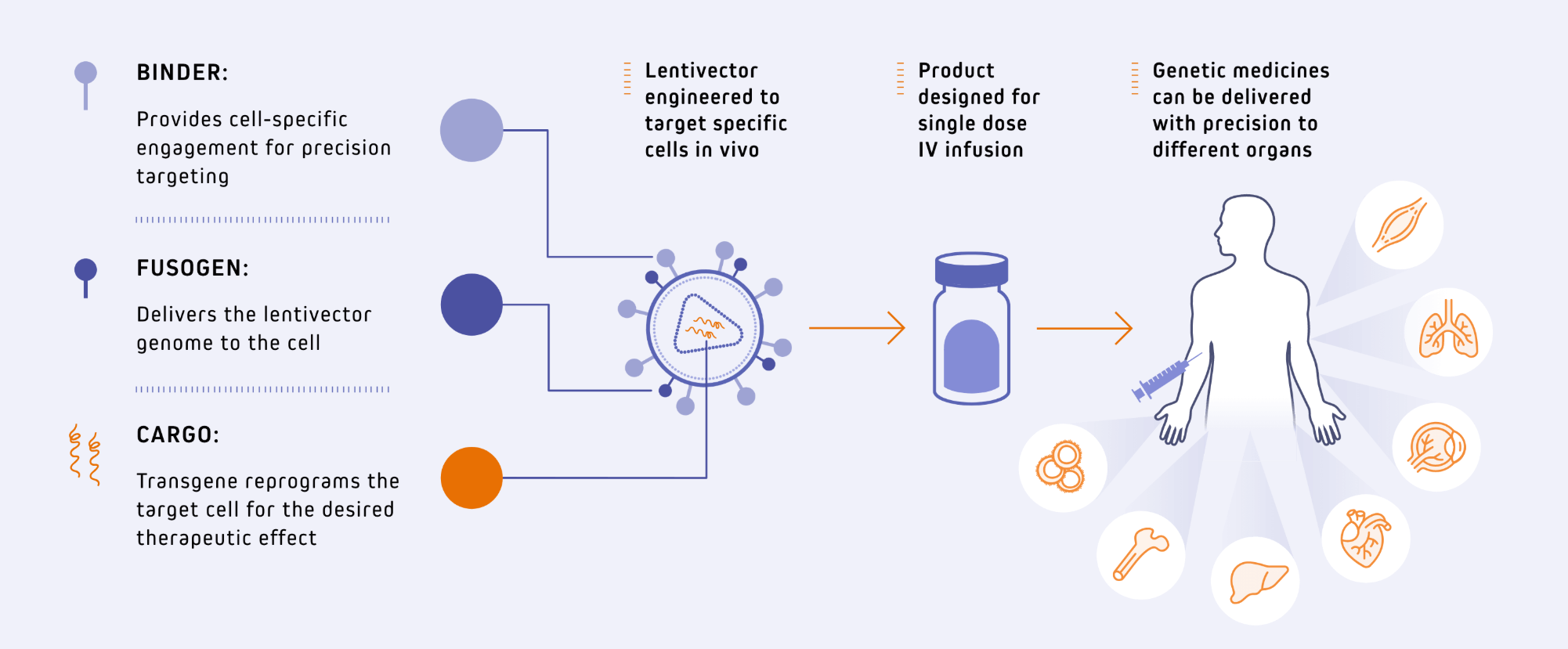
图1 Interius BioTherapeutics慢病毒体内CAR-T产品特征
Umoja Biopharma开发的VivoVec平台也是一种慢病毒体内递送和CAR-T细胞生成平台。VivoVec颗粒采用Cocal融合病毒糖蛋白进行假型化。可以抵抗人血清的灭活作用,从而提高体内稳定性,允许直接输注给患者。VivoVec产品将CD80和CD58 T细胞共刺激配体与抗CD3单链抗体(Single-Chain Fragment Variable,scFv)整合到单个多结构域融合蛋白中,不仅实现了对T细胞的高特异性靶向,还使颗粒具备了在体内结合、活化和转导T细胞的能力。Umoja的首个项目UB-VV111编码靶向CD19的CAR,同时携带雷帕霉素激活的细胞因子受体(Rapamycin-Activated Cytokine Receptor,RACR)。非人灵长类动物模型研究表明,单次输注后经淋巴结内或静脉给药,CAR-T细胞占循环T细胞的比例最高可达65%,B细胞可快速且持久地耗竭。2024年7月,Umoja已在美国和国际启动I期临床试验,用于治疗B细胞恶性肿瘤。2024年1月,艾伯维(Abbvie)宣布获得UB-VV111的开发和商业化选择权。Umoja的第二个核心研发项目是UB-VV400,编码靶向CD22的CAR,同样与RACR系统联合使用。该产品在人源化小鼠模型中获得了临床前概念验证。Umoja与中国合作伙伴驯鹿生物(IASO Biotherapeutics)合作开展的研究者发起试验已于2024年底启动,重点关注B细胞恶性肿瘤,并进一步探索其在自身免疫性疾病中的应用。
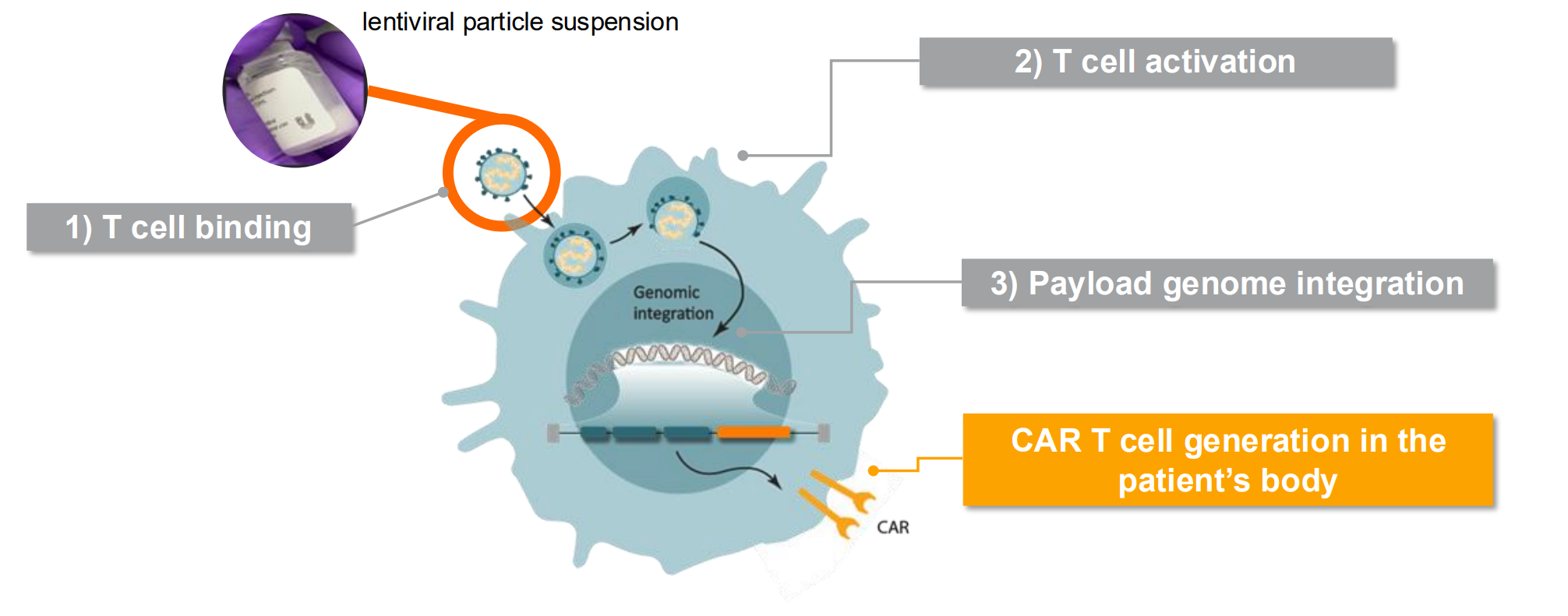
图2 Umoja Biopharma慢病毒体内CAR-T产品特征
EsoBiotec/深圳普瑞金(Shenzen Pregene)开发了一种基于第三代自灭活、VSV-G蛋白靶向缺陷型慢病毒载体的抗BCMA CAR产品,该产品具有工程化包膜(ENaBL-T),通过特异性识别TCRαβ实现T细胞靶向,同时通过主要组织相容性复合物(Major Histocompatibility Complex,MHC)I类分子缺失和CD47表达实现免疫隐身,并携带由T细胞特异性启动子驱动的载荷。该技术可有效转导静息态和活化态T细胞,在多发性骨髓瘤模型中获得了临床前概念验证。在临床研究中,首例接受治疗的多发性骨髓瘤患者实现了疾病缓解。值得注意的是,在治疗后28天即完成了快速应答,这表明其无需长期CAR暴露即可快速实现完全缓解。最近的报道显示,4名多发性骨髓瘤患者(包括上述首例患者)均实现了应答。患者1在第2个月达到严格完全缓解,所有髓内和髓外病灶消失;患者2在D28达到严格完全缓解;患者3和4达到部分缓解,骨髓微小残留病灶阴性。这一结果推动阿斯利康(AstraZeneca)收购了EsoBiotec,显示了大型制药公司对体内CAR疗法的兴趣。
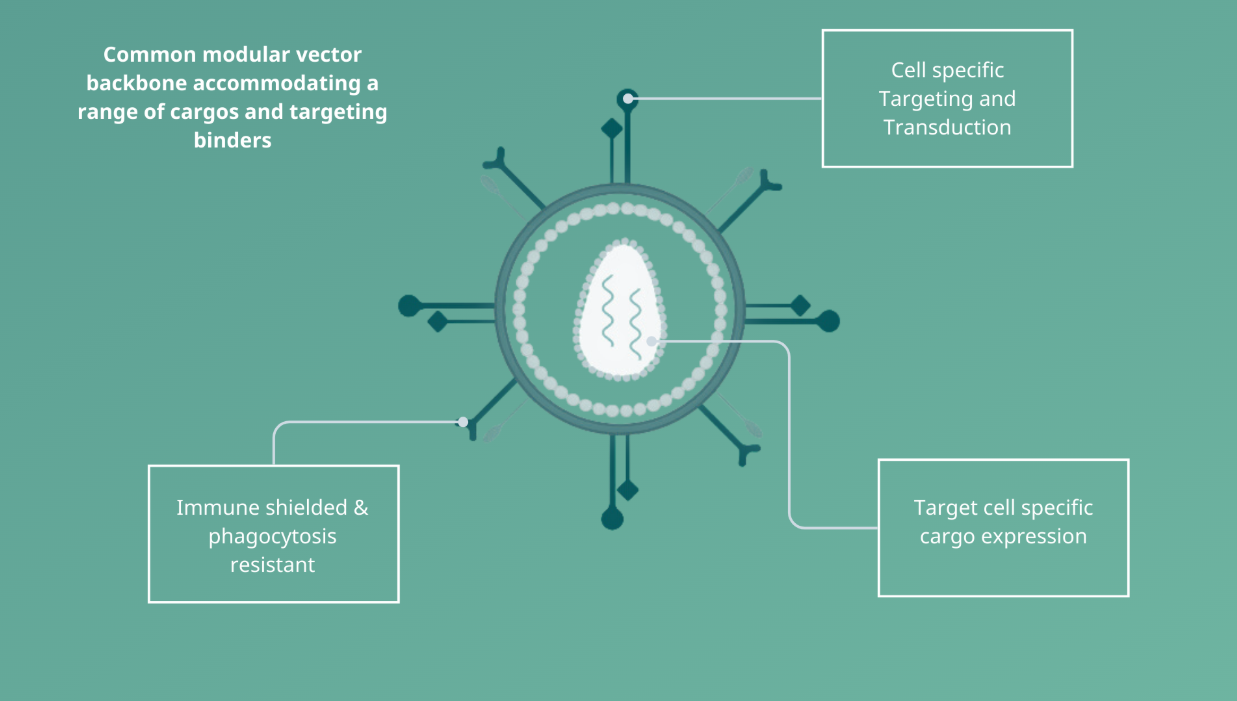
图3 EsoBiotec慢病毒体内CAR-T产品特征
Kelonia Therapeutics是一家临床阶段的生物技术公司。致力于利用其体内基因定位系统(iGPS)开发创新治疗方法。iGPS使用包膜改良、无复制能力、自失活的慢病毒载体颗粒,通过包膜修饰提高体内基因转移效率,并利用趋向性分子促进组织特异性递送,从而实现高度精准的体内基因递送和T细胞靶向。领先候选产品KLN-1010针对BCMA靶点,用于复发/难治性多发性骨髓瘤。KLN-1010 在小鼠多发性骨髓瘤模型中展现出强效肿瘤控制效果,且能诱导生成高比例记忆表型(尤其是干细胞样记忆)的 CAR-T 细胞,提示其具有持久抗肿瘤的临床潜力。同时,KLN1010也展现出精准的 T 细胞靶向性:肝脏中主要转导 T 细胞、极少非靶细胞,卵巢生殖细胞无转导,既保证疗效也提升了安全性。在2025年ASH会议上公布的首批人体数据中,4例患者全部在1个月内达到MRD阴性,CAR-T 细胞扩增在第 15 天左右达到峰值,记忆表型 T 细胞可在骨髓和血液中持续存在至治疗后 3 个月,且毒性可控。2025年11月5日,Kelonia Therapeutics宣布和强生公司达成战略合作,以推进新型体内CAR-T 细胞疗法的研发进程。
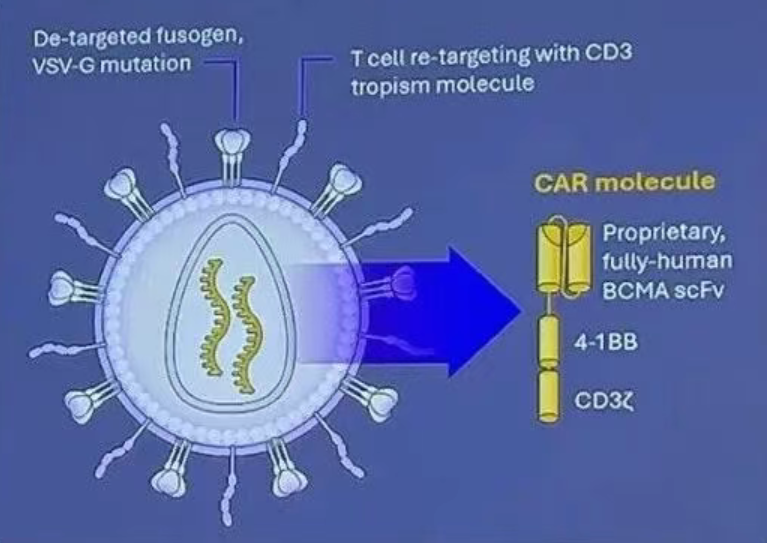
图4 Kelonia Therapeutics慢病毒体内CAR-T产品特征
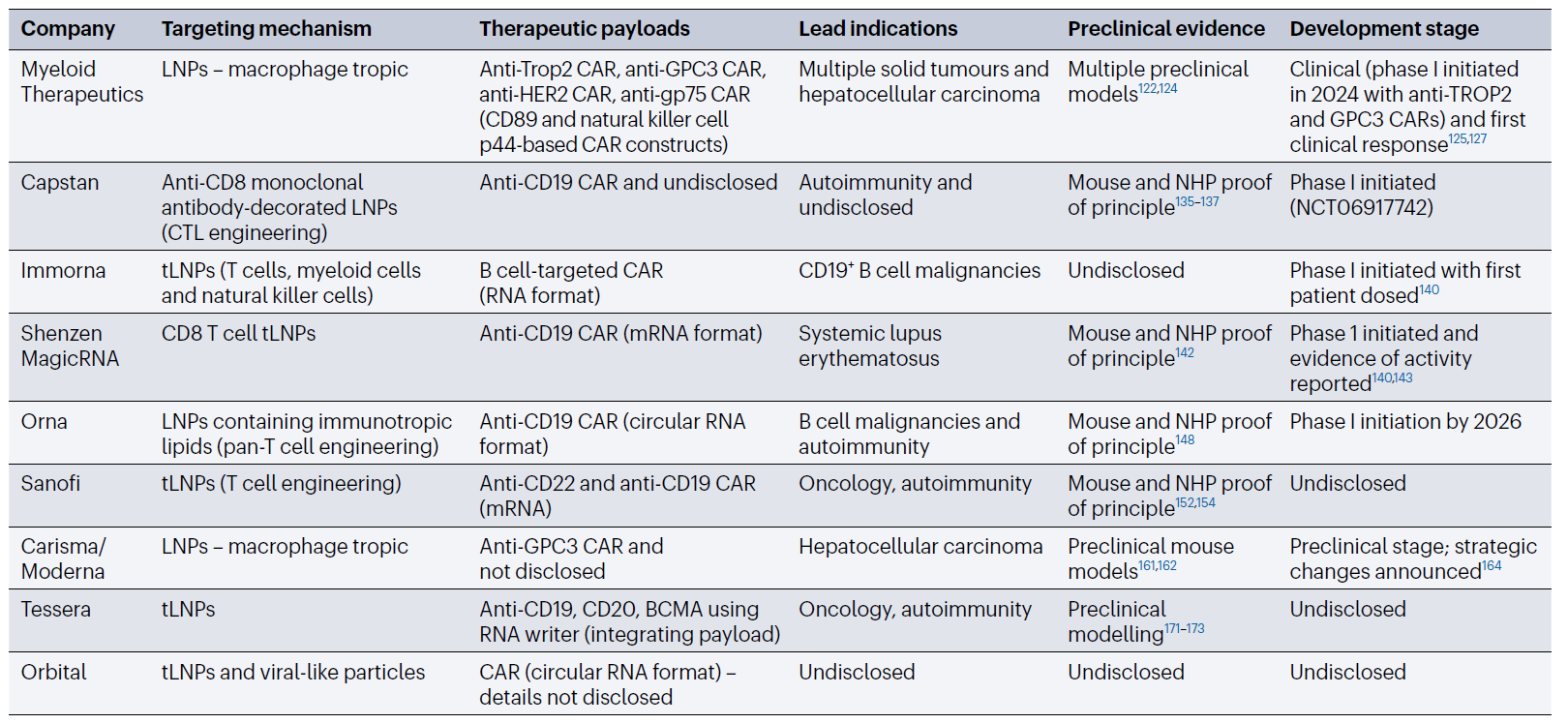
表2 LNP-RNA体内CAR-T细胞平台
CREATE Medicines(前身为 Myeloid Therapeutics)体内工程化平台可特异性靶向并活化髓系细胞,使其重新靶向肿瘤细胞。该技术利用了LNPs对髓系细胞谱系的天然嗜性,CAR设计包含截短的FcαR(CD89)与内源性FcRγ链形成多链复合物。保证其在细胞表面稳定表达,从而实现谱系特异性表达和功能。研究人员还通过对mRNA编码序列和3'非翻译区(UTR)进行修饰,以增强并延长CAR表达。在小鼠肺异种移植模型中,静脉给药TROP2 CAR mRNA-LNP可抑制肿瘤生长。在食蟹猴中,TROP2 CAR mRNA-LNPs主要被髓系细胞内化。食蟹猴输注GPC3 CAR mRNA-LNPs后观察到CAR的剂量依赖性表达,并在小鼠模型中发现抗肿瘤活性与细胞因子水平升高相关。这两款产品已进入I期临床试验:MT-302(TROP2+上皮源性恶性肿瘤R)首名患者于2023年9月完成给药,MT-302可在外周血和肿瘤微环境中实现CAR表达。MT-303(过表达GPC3的原发性或转移性肝细胞癌)于2024年7月启动给药,已显示出抗肿瘤活性,包括经过多线治疗的患者病灶缩小。在这两项研究中,给药剂量水平下耐受性良好,未观察到剂量限制毒性,且细胞因子释放综合征可控。
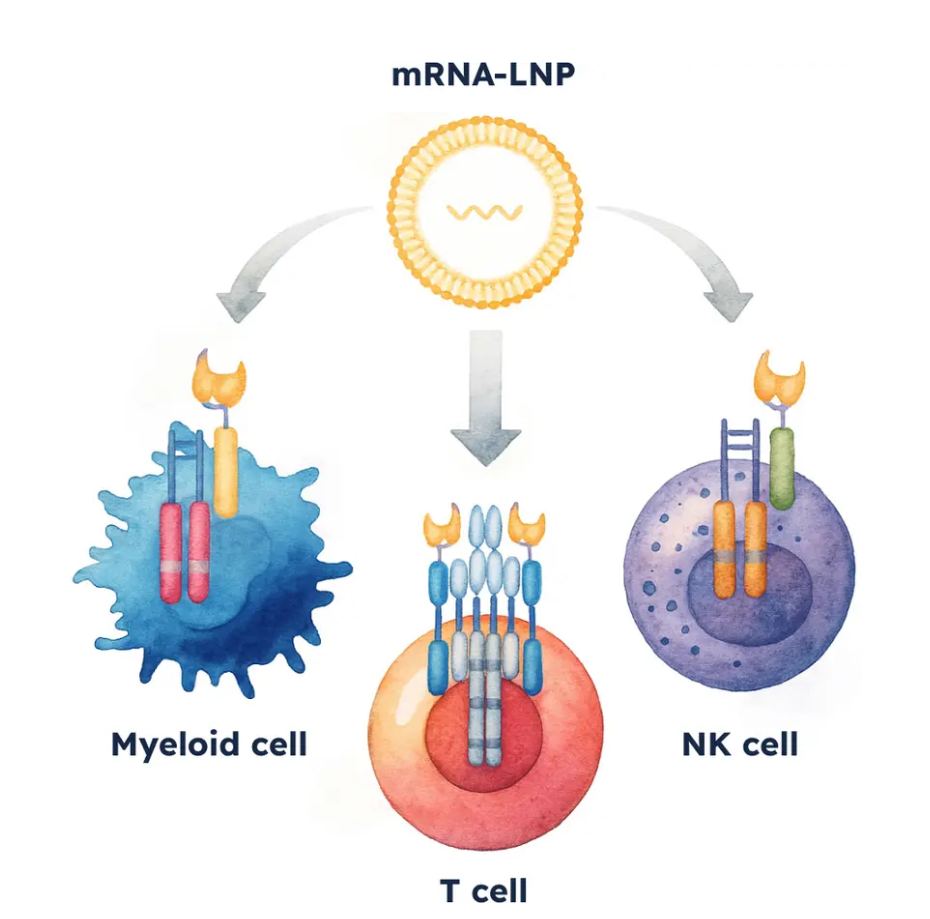
图4 CREATE Medicines mRNA-LNP技术路线
Capstan Therapeutics开发了配体修饰的LNP颗粒(CellSeeker技术),这一体内 CAR 平台包含以优化的线性 mRNA 递送的载荷,通过靶向LNP(target LNP,tLNP)进行传递。与用于mRNA疫苗的LNPs相比,tLNPs是生物降解性高、反应原性低的可电离脂质,可用于重复静脉输注。由于该mRNA工程化方法可实现CAR的瞬时和自限性表达,可避免过高或过长的靶向毒性、病毒成分引起的免疫原性以及遗传毒性,从而提升患者的可及性。Capstan抗CD19 CAR高效体外工程化来自健康人或患者的人T细胞,在人源化小鼠模型中的概念验证表明,可在体内快速工程化人CD8+ T细胞,并对原代或恶性B细胞产生强效活性。抗CD8-LNP-mRNA形式的抗CD20 CAR,能够显著减少 B 细胞,包括淋巴组织和骨髓中的记忆 B 细胞,随后以主要为幼稚 B 细胞的形式重新增殖,实现了免疫重置。今年启动了首次人体试验,Capstan 计划开发更广泛的体内 CAR 产品组合,适用于自身免疫性疾病和其他类别适应症。近日,艾伯维(Abbvie)宣布收购Capstan Therapeutics,显示了大型药企对这一快速发展领域的兴趣。
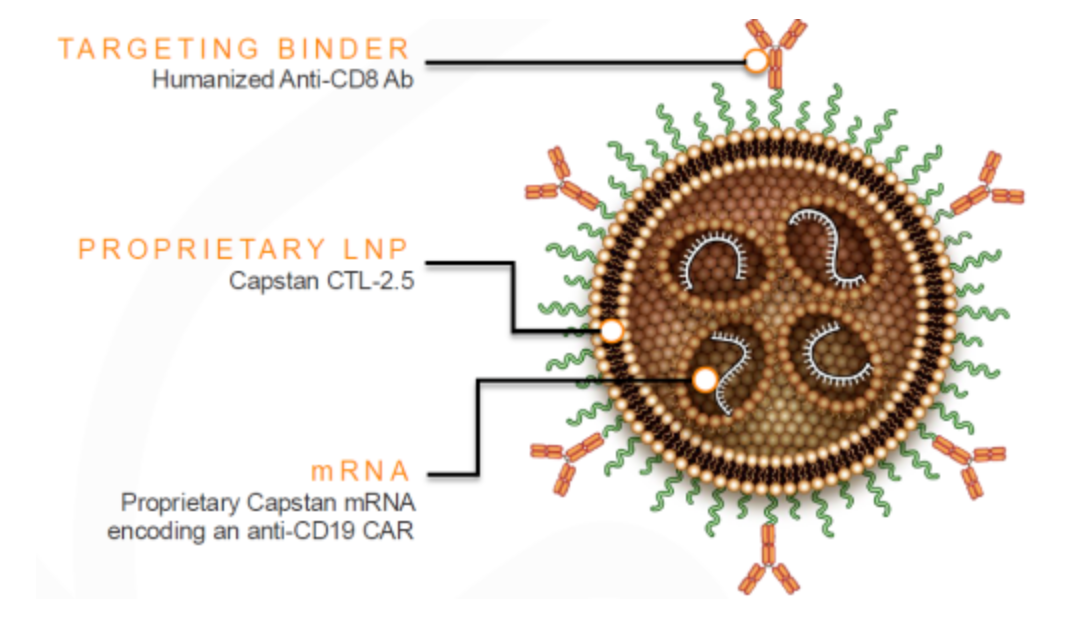
图5 Capstan Therapeutics mRNA-LNP技术路线
虹信生物(MagicRNA)抗CD19 CAR的CD8-tLNP(HN2301)已推进至临床阶段。其Enc-LNP平台包含专有的抗体片段和可电离脂质。临床前证据显示,在人CD8转基因狼疮肾炎模型中,替代抗CD19 CAR具有活性;非人灵长类动物中,在输注抗CD20 CAR替代产品中观察到“免疫重置”的迹象。研究者发起的临床试验正在评估HN2301治疗复发难治性系统性红斑狼疮患者的安全性、疗效及平台的广泛适用性。该方法已证实可在体内工程化抗CD19 CD8+ CAR-T细胞,同时观察到B细胞耗竭、与靶向活性相关的细胞因子产生,以及系统性红斑狼疮患者自身抗体滴度降低所体现的临床相关生物标志物活性。今年9月发表的文章中披露,5例患者接受体内HN2301后,不良事件均为1–2级,未观察到3–4级毒性。每剂 HN2301 输注后 6 h 出现尖峰(最高约 60–80 %),随后 48–72 h 回落至基线。在接受首次治疗后的 6 小时内,接受 2 毫克剂量治疗的患者(患者 1 和 2)循环 B 细胞显著减少,而接受 4 毫克剂量治疗的患者(患者 3、4 和 5)循环 B 细胞则完全耗尽(每微升少于 1 个 B 细胞),且这种耗尽状态一直持续到给药后 7-10 天。在最后一次随访(治疗 3 个月后),所有 5 名患者的系统性红斑狼疮疾病活动指数 2000 评分均有所下降,表明他们的疾病活动度降低。近日,虹信生物获得腾讯的入股。
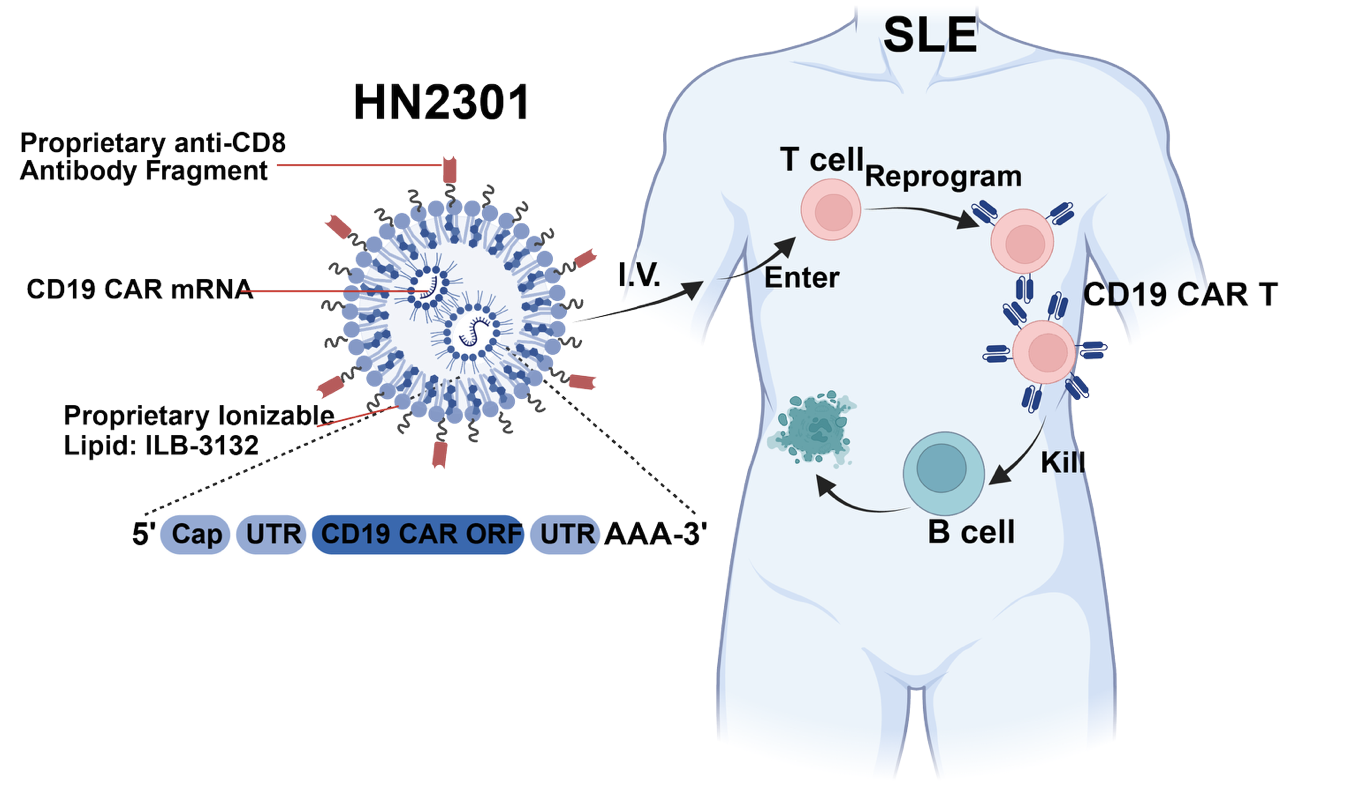
图6 虹信生物工程化细胞靶向脂质纳米颗粒
本篇内容系统地梳理了体内CAR-T细胞治疗的临床开发进展,这些进展标志着体内CAR-T正从概念走向临床验证,为肿瘤与自身免疫性疾病治疗提供了新的可能。下篇将为大家深入介绍熙宁|精翰生物针对体内CAR-T生物分析策略与典型案例,从方法开发、验证到临床样本分析的全流程实践,敬请期待。
针对体内CAR-T的临床生物分析和生物标志物检测需求,熙宁|精翰生物可提供从PK/PD、免疫原性、安全性评估到探索性生物标志物的一站式检测服务,凭借其全平台技术能力、丰富细胞治疗项目经验、自主方法学与合规体系,为体内CAR-T的临床试验提供可靠的分析支持。欢迎您后台留言咨询。
参考文献:
[1] Bot A, Scharenberg A, Friedman K, et al. In vivo chimeric antigen receptor (CAR)-T cell therapy. Nat Rev Drug Discov. Published online September 30, 2025.
[2] Li YR, Zhu Y, Halladay T, Yang L. In vivo CAR engineering for immunotherapy. Nat Rev Immunol. 2025;25(10):725-744.
[3] Xu J, Liu L, Parone P, et al. In-vivo B-cell maturation antigen CAR T-cell therapy for relapsed or refractory multiple myeloma. Lancet. 2025;406(10500):228-231.
[4] Simon H, Phoebe JH, Sueh-Li L, et al. Minimal residual disease (MRD)-negative outcomes following a novel, in vivo gene therapy generating anti–B-cell maturation antigen (BCMA) chimeric antigen receptor (CAR)-T cells in patients with relapsed and refractory multiple myeloma (RRMM): Preliminary results from inMMyCAR, the first-in-human phase 1 study of KLN-1010. Blood 2025; 146 (Supplement 2): LBA–1.
[5] Wang Q, Xiao ZX, Zheng X, et al. In Vivo CD19 CAR T-Cell Therapy for Refractory Systemic Lupus Erythematosus. N Engl J Med. 2025;393(15):1542-1544.
[6] https://interiusbio.com/platform/
[7] Nicolai et al, Blood. 2024 Aug 144(9):977-987
[8] https://www.esobiotec.com/science/
[9] https://createmedicines.com/
[10] https://www.abbvie.com/capstan-therapeutics.html
[11] https://cn.magicrna.com/elnp/93.html