



近年来,基因组学、流行病学、孟德尔随机研究均显示,Lp(a)升高是多种CVD包括CAD、缺血性脑卒中和钙化性主动脉瓣狭窄(CAVS)等疾病的独立危险因素[1],会显著增加心肌梗死、卒中等心血管疾病的发病及死亡风险,甚至全因死亡风险[2]。虽然血清中Lp(a)浓度主要与遗传相关,且正常人群中Lp(a)水平呈明显的偏态分布,并伴有一定的地域和种族差异。但是通常以300 mg/L为切点,高于此水平者,ASCVD风险显著增加[3]。因此,Lp(a)的检测有助于对因Lp(a)升高而导致的动脉粥样硬化及血栓风险的患者进行可靠的诊断和分类,对于提高CVD的风险评估准确率,改善患者预后具有重要意义[4]。
Lp(a)分为脂质部分和蛋白部分,蛋白部分主要由载脂蛋白B100(ApoB100)和载脂蛋白a[Apo(a)]以二硫键共价结合形成[5],如图1所示。其中Apo(a)是一种高度糖化且肽链长度不一的亲水蛋白质,占Lp(a)总量的25%~40%。不同个体间Apo(a)的糖化程度和可变区肽链长度存在较大的差异,且大多数个体一般携带两种不同的Apo(a)(父源、母源),故导致Lp(a)具有显著且复杂的多态性[6]。
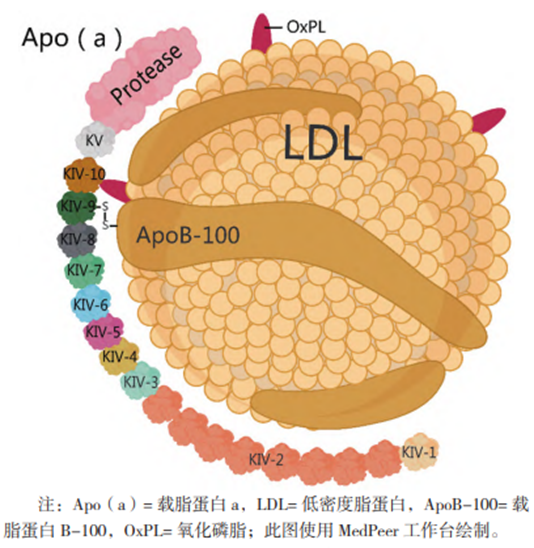
图1 脂蛋白a结构
Lp(a)的多态性使得定量检测Lp(a)面临着巨大挑战。因为在定量检测过程中,无论标准品或校准品中的Apo(a)是固定肽链长度单一物质,还是多种肽链长度的Apo(a)异构体按照一定比例混合的混合物,均无法保证标准品或校准品中Apo(a)分子与样品中Apo(a)分子之间的差异可忽略不计。当差异存在时,由于Apo(a)异构体的免疫反应性和分子量不同,极易产生测量误差,难以准确定量,无法形成标准化的结果。
为了应对上述挑战,在临床实践中一般采用以下策略:
1、使用摩尔浓度单位,即采用nmol/L作为Lp(a)的报告单位。相较于传统的质量浓度单位,如mg/L,摩尔浓度单位表明测量的是Lp(a)的颗粒数,而不是Lp(a)的质量,因此不受Apo(a)异构体分子量的影响;
2、使用对Apo(a)可变区变化不敏感的抗体,对Lp(a)进行定量检测,使得样品结果不受Apo(a)异构体的免疫反应性差异的影响;
3、选用与检测方法适配的标准品或校准品,使得整个检测体系可溯源至WHO/IFCC SRM-2B。
4、在满足上述条件后,应当尽可能的优化方法,使其可以耐受干扰物质对结果的影响,比如与Lp(a)结构类似的纤溶酶原、游离的Apo(a)、ApoB 100、高脂、溶血等。
目前Lp(a)的主流检测方法有两种,分别为胶乳免疫比浊法和ELISA法,其中胶乳免疫比浊法是目前的主流方法。该方法通过物理吸附或者化学偶联的方式,将Lp(a)抗体包被在胶乳颗粒表面,通过抗原抗体免疫反应,与样品中的Lp(a)结合形成不溶的免疫复合物。通过检测透射光或散射光强度的变化,来实现Lp(a)的定量检测。此类方法大多是选用对Apo(a)可变区的变化不敏感的多克隆抗体进行Lp(a)的检测。如罗氏的脂蛋白(a)检测试剂盒(乳胶增强免疫比浊法)、迈瑞的脂蛋白(a)[Lp(a)]测定试剂盒(胶乳免疫比浊法)等。
熙宁|精翰生物以迈瑞的脂蛋白(a)[Lp(a)]测定试剂盒(胶乳免疫比浊法)为基础,经过一系列调整和优化后,建立了基于生化平台的自主产权的Lp(a)定量检测方法(简称为生化方法)。该方法在参照GLP/GCP/GCLP运行的熙宁实验室中,进行了完整的GLP验证,包括但不限于准确度与精密度、平行性、干扰物质、钩状效应、稳定性等验证,并在临床样品的比对中,展现出了良好的一致性。具体的方法验证参数如下:

ELISA法作为另一种主流的检测方法,其主要检测原理为双抗体夹心检测法,即将包被抗体以物理吸附的方法固定于微孔板表面,然后加入待测样品,再加入酶标记检测抗体,形成固定于微孔板表面的双抗体夹心免疫复合物。最后用TMB底物显色,通过检测微孔板中颜色的变化,来进行Lp(a)的检测。其中包被抗体一般选择仅识别Apo(a)的KIV-8或KIV-9位点的抗体或对Apo(a)可变区变化不敏感的多克隆抗体,检测抗体一般选择抗ApoB抗体。也可以包被抗体选择抗ApoB抗体,检测抗体选择抗Apo(a)抗体。并无研究表明两种抗体配对方式之间的检测结果有显著差异。检测抗体除了标记HRP等酶以外,还可以通过标记生物素或者钌,来放大检测信号,从而进一步提升方法的检测灵敏度。
熙宁|精翰生物在参考了一系列文献的基础上,同样建立了基于ELISA平台的自主产权的Lp(a)定量检测方法(简称为ELISA方法)。该方法在参照GLP/GCP/GCLP运行的熙宁实验室中,进行了完整的GLP验证,包括但不限于准确度与精密度、平行性、干扰物质、钩状效应、稳定性等验证,并在临床样品的比对中,展现出了良好的一致性。具体的方法验证参数如下:

生化方法因为其检测原理的局限性,即该方法仅检测Lp(a)的Apo(a),故其实际检测物质为总Apo(a)蛋白,无法区分游离的Apo(a)蛋白和Lp(a)。但有研究表明,Apo(a)蛋白主要以Lp(a)的形式存在于人体血液中,游离的Apo(a)仅占总Apo(a)的约5%。因此在常规检测情况下,总Apo(a)蛋白含量与Lp(a)含量基本等同。
ELISA方法一般既检测Lp(a)的Apo(a),也检测ApoB,故其实际检测物质为intact Lp(a),不受游离的Apo(a)蛋白干扰。在靶向Lp(a)药物研究中,使用了靶向Lp(a)药物的患者,尤其是使用了限制Lp(a)组装的小分子药物的患者,其血液中的游离Apo(a)在总Apo(a)中比例可能会产生显著变化。此时总Apo(a)蛋白含量与Lp(a)含量的差异不可忽略。
根据既往熙宁|精翰生物的分析经验,在靶向Lp(a)药物的临床前研究中,比如Lp(a)的组装实验、小鼠或食蟹猴的药理研究中,建议使用ELISA方法,生化方法的检测结果可能难以满足研究预期。由于生化方法的自动化程度高,且在临床实践中的应用更加广泛并形成了统一的专家共识,因此建议在临床研究的入组筛选期,使用生化方法作为标准方法。在评估药效时,可根据药物的作用机理,来评估是否需要使用ELISA方法作为补充方法。礼来的研究表明,在评估小分子Lp(a)形成抑制剂(如muvalaplin)的药效时,生化方法会显著低估药物的疗效。在评估可降低Lp(a)的小干扰RNA类型药物(如lepodisiran)的药效时,生化方法与ELISA方法无显著差异[7]。
熙宁|精翰生物临检平台凭借多次顺利通过室间质评(EQA)的扎实资质,可提供全面契合 GCP/GLP/GCLP 质量规范的生物样品检测及分析服务。平台配齐全自动生化检测仪、全自动化学发光测定仪、全自动电化学发光分析仪、全血细胞检测仪、全自动凝血检测仪、全自动流式荧光免疫测定仪等一系列先进检测设备,构建起多维度、高精度的检测技术支撑体系。
临检平台始终聚焦客户核心需求,致力于为客户提供及时响应的安全性评估及临床检测一体化解决方案,服务范畴覆盖常规生化检测、血液学分析、免疫学检测、特殊蛋白测定等核心领域,为内分泌系统疾病、心血管疾病、感染性疾病、肿瘤、自身免疫性疾病、性激素相关疾病、代谢性疾病等多个方向的临床研究,提供专业、高效的技术支持,助力新药研发项目稳步推进。
参考文献:
[1]北京心脏学会,李建军,马长生.脂蛋白(a)与心血管疾病风险关系及临床管理的专家科学建议[J].中国循环杂志, 2021, 36(12):10-10.
[2]Langsted A, Kamstrup PR, Nordestgaard BG. High lipoprotein(a) and high risk of mortality[J]. Eur Heart J. 2019; 40(33): 2760-2770.
[3]鄢盛恺. 关于临床血脂测定的建议[J]. 中华检验医学杂志,2003, 26(3): 182‐184.
[4]Kronenberg F, Tsimikas S. The challenges of measuring lp(a): a fight against hydra?[J]. Atherosclerosis, 2019, 289: 181-183.
[5]Cegla J, Neely RDG, France M, et al. HEART UK consensus statement on lipoprotein(a): a call to action[J]. Atherosclerosis, 2019,291: 62-70.
[6]Tsimikas S. A test in context: lipoprotein(a): diagnosis, prognosis,controversies, and emerging therapies[J]. J Am Coll Cardiol, 2017,69(6): 692-711.
[7]Craig A, Swearingen,John H, Sloan,Grace M, Rhodes et al. Measuring Lp(a) particles with a novel isoform-insensitive immunoassay illustrates efficacy of muvalaplin.[J] .J Lipid Res, 2024, 66:100723.