



在肿瘤精准治疗飞速迭代的当下,靶蛋白降解技术(TPD)凭借分子胶和PROTAC两大核心技术赛道,突破传统小分子靶向药的作用局限,攻克众多“不可成药”靶点难题;同时还为炎症、神经系统等多类疾病开辟全新治疗方向。这类药物依托机体泛素-蛋白酶体系统,特异性降解致病靶蛋白,其作用机制与传统小分子抑制剂截然不同。而多元化的NGS(下一代测序)技术体系,更为这类药物的早期临床药效评估、机制验证、获益人群筛选提供了硬核技术支撑。
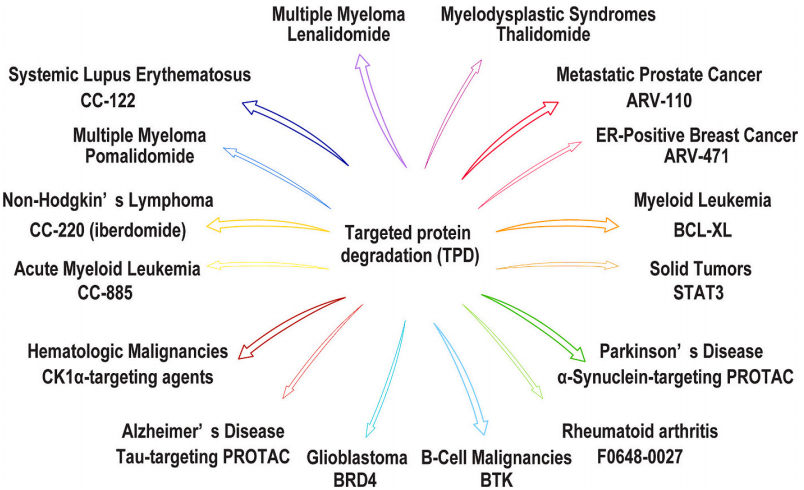
图1 分子胶和PROTACs的治疗应用
NGS髓系肿瘤58基因panel,直击临床药效关键数据
在髓系恶性肿瘤等克隆性疾病中,驱动基因突变(如FLT3、TP53、JAK2等)是恶性造血克隆的分子标志。NGS技术能够在治疗过程中连续监测这些突变的变异等位基因频率(VAF),为药效评估提供精确量化指标。
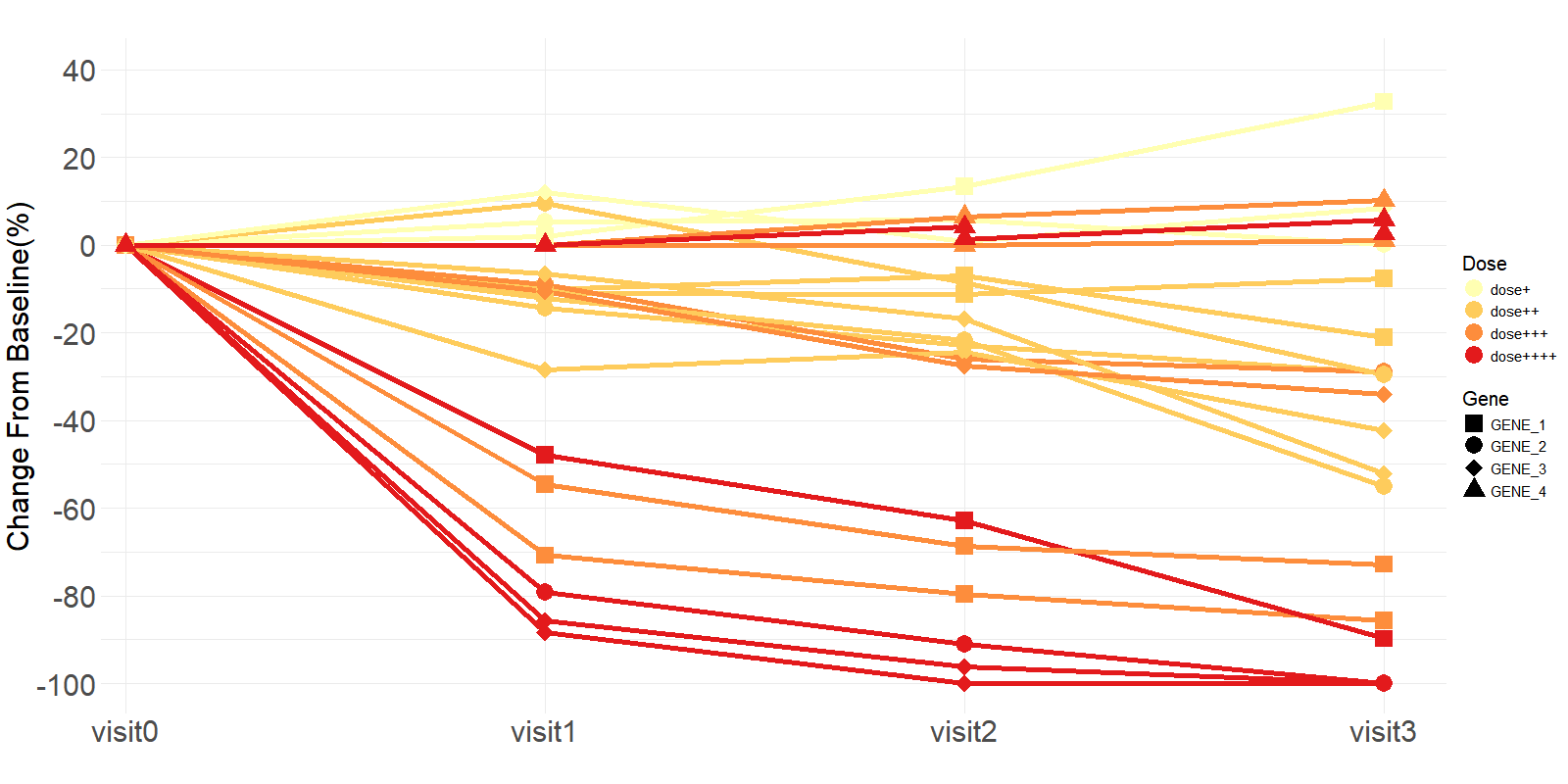
图2 驱动基因突变动态变化示意图
精翰部分临床样品和模拟数据展示。采用NGS髓系肿瘤58基因panel在筛选期和给药后各时间点监测。
驱动基因突变频率变化趋势总结:
➢
利用NGS多基因检测技术,能够同时追踪不同基因突变的动态变化,为全面评估治疗响应提供了可靠依据。
➢
低剂量组各驱动基因突变VAF相对稳定,清晰呈现剂量-效应关系。
➢
高剂量组在治疗早期观察到显著VAF下降趋势,证实与临床部分缓解反应相关。
➢
高剂量组在治疗中后期,驱动突变VAF接近检测下限,提示实现完全分子学缓解。
➢
高剂量组携带部分基因突变VAF水平整体保持稳定,且呈轻度上升趋势,提示可能存在耐药相关的基因变异。
NGS髓系肿瘤58基因panel聚焦肿瘤驱动基因、药效通路关键位点,全面解析髓系肿瘤患者基线基因突变图谱,区分不同基因背景亚型患者。精准筛选对分子胶药物敏感的优势人群,为临床试验入组分层、个体化给药奠定基础。
纵向追踪不同随访时间点、不同剂量组患者的关键基因特征变化,数据直观印证药物剂量依赖性、时间累积效应:高剂量组靶标相关基因调控更显著,从基因层面佐证分子胶药物精准降解靶蛋白、激活抑癌通路的核心药理机制。
拓展赋能:多维度NGS技术,全方位丰富药效学研究体系
·
转录组RNA-seq:解析全局通路调控
研究团队对PROTAC处理的早衰症患者细胞进行RNA-seq全转录组分析,对比未处理组,发现处理组细胞周期、DNA损伤修复、线粒体功能相关基因表达显著改变,从分子层面验证PROTAC可全面改善病理表型。
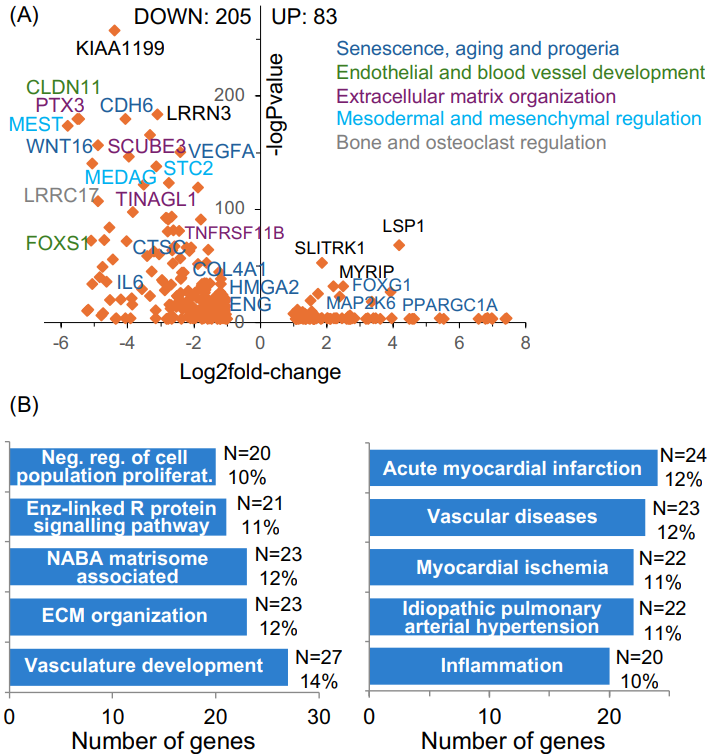
图3 基于RNA-seq的差异表达基因及通路富集分析
·
单细胞NGS:靶点发现和降解效应评估
scRNA-seq技术在分子层面解析了RIT1突变或LZTR1缺失如何驱动造血干细胞的异常扩增和恶性转化,从而为后续使用PROTAC药物靶向RAS蛋白提供了关键的机制依据和理论支撑。
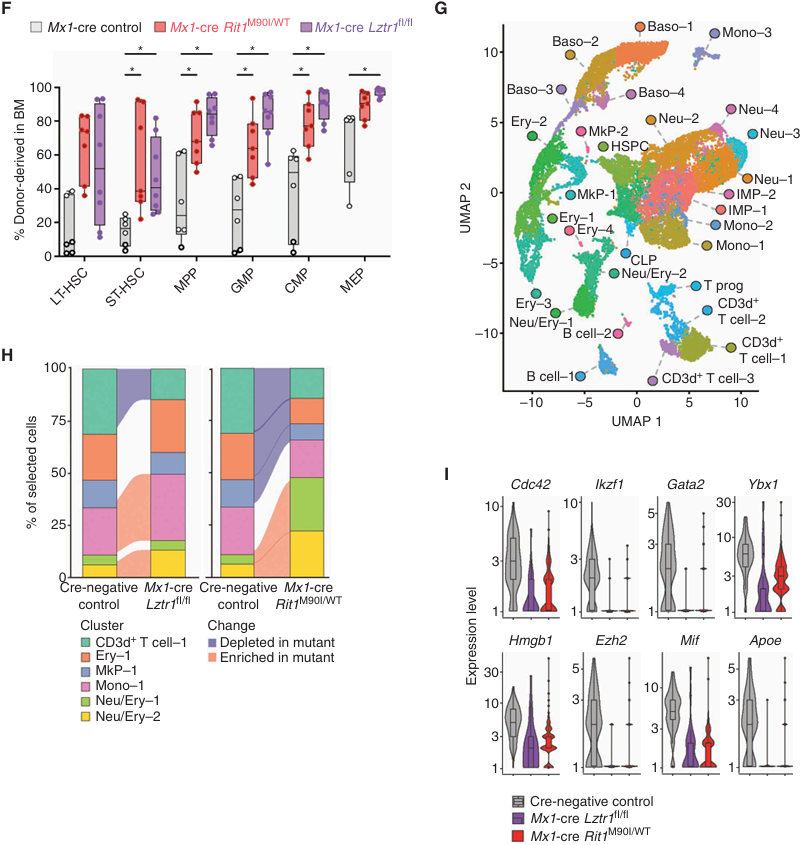
图4 基于scRNA-seq技术的不同处理组单细胞转录组图谱分析
熙宁|精翰NGS检测平台拥有经验丰富的研发人员和专业的生信团队,实验室配备有Illumina NextSeq测序仪、Covaris M220基因打断仪和安捷伦自动化电泳仪4150等仪器,可满足各类生物标志物检测和伴随诊断试剂盒开发需求。
熙宁|精翰NGS髓系肿瘤58基因panel是一种基于多重扩增建库技术,包含58个基因,其中18个基因的CDS区域和40个基因的热点突变区域,可同时检测单核苷酸变异、插入缺失和FLT3-ITD。主要用于髓系肿瘤(包括AML、MDS、MPN、MDS/MPN 等)的疾病诊断分型、预后评估、用药指导和遗传筛查。
除了58基因panel外,熙宁|精翰NGS平台还可支持免疫组库测序(TCR-Seq/BCR-Seq)、慢病毒整合位点检测、血液肿瘤/实体瘤微小残留病灶(MRD)检测、HLA/KIR分型检测、实体瘤/血液肿瘤靶向580/641/60基因检测、全基因组/外显子组检测、RNA-Seq转录组测序、单细胞转录组测序与免疫组库测序以及CDx产品开发与注册申报等服务,全面支撑药物的安全性评估、治疗效果评估、入组筛查、生物标志物的探索和伴随诊断产品的开发等,在药物研发的各个环节发挥重要作用。
参考文献:
[1] E Eladl O. Molecular glues and PROTACs in targeted protein degradation: mechanisms, advances, and therapeutic potential. Biochem Pharmacol. 2025 Dec;242(Pt 3):117297. doi: 10.1016/j.bcp.2025.117297. Epub 2025 Sep 2. PMID: 40907798.
[2] Macicior-Michelena J, Telechea M, Fernández D, García-Martín A, Canales Á, Ortega-Gutiérrez S. First Generation Proteolysis Targeting Chimeras (PROTACs) for the Treatment of Progeria. Adv Sci (Weinh). 2026 Mar 23:e21608. doi: 10.1002/advs.202521608. Epub ahead of print. PMID: 41869760.
[3] Chen S, Vedula RS, Cuevas-Navarro A, Lu B, Hogg SJ, Wang E, Benbarche S, Knorr K, Kim WJ, Stanley RF, Cho H, Erickson C, Singer M, Cui D, Tittley S, Durham BH, Pavletich TS, Fiala E, Walsh MF, Inoue D, Monette S, Taylor J, Rosen N, McCormick F, Lindsley RC, Castel P, Abdel-Wahab O. Impaired Proteolysis of Noncanonical RAS Proteins Drives Clonal Hematopoietic Transformation. Cancer Discov. 2022 Oct 5;12(10):2434-2453. doi: 10.1158/2159-8290.CD-21-1631. PMID: 35904492; PMCID: PMC9533010.